Expert médical de l'article
Nouvelles publications
Hépatite à cytomégalovirus
Dernière revue: 05.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
Épidémiologie
L'infection à CMV est répandue. 70 à 80 % des adultes présentent des anticorps neutralisants dans leur sang. Le virus est excrété dans les urines chez 4 à 5 % des femmes enceintes, détecté dans les frottis cervicaux chez 10 % des femmes et dans le lait maternel chez 5 à 15 % des mères allaitantes. Parmi les nouveau-nés décédés de causes diverses, des signes d'infection généralisée à CMV sont détectés chez 5 à 15 %. L'hépatite à cytomégalovirus représente 1 % des cas d'hépatite ictérique aiguë d'origine virale. Cependant, la prévalence de l'hépatite à cytomégalovirus dans son ensemble n'a pas été étudiée à ce jour.
La source de l'infection à CMV est uniquement une personne, malade ou porteuse du virus. La transmission se fait par contact, plus rarement par gouttelettes en suspension dans l'air et par voie entérale. De plus, l'infection peut se produire par voie parentérale, notamment lors de transfusions sanguines. Cette voie de transmission semble plus fréquente qu'on ne le croit, comme le confirme la détection fréquente du cytomégalovirus chez les donneurs (jusqu'à 60 %). La voie transplacentaire de transmission de l'infection a été prouvée de manière fiable. L'infection du fœtus se produit par la mère, porteuse du virus. L'infection se transmet directement par le placenta ou intrapartum lors du passage de l'enfant dans les voies génitales. Les nouveau-nés peuvent être infectés par le lait maternel.
Dans l'hépatite à cytomégalovirus, les voies d'infection prédominantes sont apparemment parentérales et périnatales, lorsque le cytomégalovirus pénètre directement dans le sang, contournant l'appareil lymphoïde du patient.
Causes hépatite à cytomégalovirus
Le cytomégalovirus, membre de la famille des Herpesviridae, a été isolé en 1956 par M. Smith. Selon la classification moderne, il est appelé virus de l'herpès humain de type 5 (HHV5). Actuellement, deux sérotypes de cytomégalovirus sont connus. Morphologiquement, il est similaire au virus de l'herpès simplex. Le virion contient de l'ADN et a un diamètre de 120 à 140 nm. Il est bien cultivé en culture de fibroblastes embryonnaires humains. Le virus se conserve bien à température ambiante et est sensible à l'éther et aux désinfectants. Son effet interféronogène est faible. Le cytomégalovirus est exclusivement humain. Les fœtus et les nouveau-nés sont particulièrement sensibles au virus.
Pathogènes
Pathogénèse
La pathogénèse de l'hépatite à cytomégalovirus reste encore mal connue. Traditionnellement, on pense que le CMV affecte principalement les voies biliaires, entraînant le développement d'une hépatite cholestatique. Cependant, un effet cytopathique direct du CMV sur le parenchyme hépatique est admis. Certains considèrent le cytomégalovirus comme un agent hépatotrope indéniable. Dans ce cas, des lésions hépatiques peuvent être observées aussi bien en cas d'infection congénitale qu'acquise à CMV.
Dans la formation de lésions hépatocytaires isolées lors d'une hépatite à cytomégalovirus, l'entrée directe de l'agent pathogène dans le sang (mécanisme parentéral d'infection) peut jouer un rôle important. Dans ce cas, le virus ne pénètre pas dans le système lymphatique, et donc dans les ganglions lymphatiques régionaux, et encore moins s'y multiplie. L'agent pathogène apparaît immédiatement dans la circulation sanguine, d'où il pénètre dans le parenchyme hépatique. Cette phase de la chaîne pathogénique est communément appelée diffusion parenchymateuse. Dans ce cas, le virus peut pénétrer immédiatement dans les hépatocytes, où il trouve les conditions nécessaires à sa reproduction.
Dans la pathogenèse de l'hépatite à cytomégalovirus isolé, le rôle des différents génotypes de cytomégalovirus, ainsi que le polymorphisme des gènes candidats du complexe majeur d'histocompatibilité (système HLA) sur le chromosome 6 d'un individu sensible, ne peuvent être exclus.
Pathomorphologie
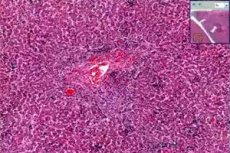
Les modifications morphologiques de l'hépatite aiguë à cytomégalovirus chez l'adulte sain se caractérisent par une combinaison de granulomes intralobulaires avec une infiltration sinusoïdale par des cellules mononucléaires, ainsi que par une inflammation périportale. La nécrose hépatocytaire peut être légère.
Chez les adultes immunodéprimés (ayant subi une transplantation rénale) atteints d'hépatite chronique à cytomégalovirus, on observe une fibrose périportale et périsinusoïdale, une infiltration cellulaire mixte, un gonflement des hépatocytes et des signes de cholestase. Aux premiers stades de la maladie, des antigènes du cytomégalovirus sont détectés dans les cellules sinusoïdales hépatiques, résultat de la dissémination hématogène du virus. On observe également des modifications nécrotiques et dystrophiques des hépatocytes, une infiltration lymphocytaire et une activation des cellules de Kupffer, tandis que la transformation cellulaire spécifique est rare. Chez ces patients, l'hépatite à cytomégalovirus s'accompagne d'un syndrome cholestatique et d'un syndrome de disparition des voies biliaires. Dans ce cas, une antigénémie pp65 et de l'ADN du CMV sont détectés dans les hépatocytes, et des signes de cirrhose hépatique peuvent être observés.
Outre les modifications classiques caractéristiques de l'hépatite virale, les patients atteints d'une atteinte hépatique due au cytomégalovirus peuvent présenter de petits agrégats de leucocytes polynucléaires neutrophiles, souvent localisés autour de l'hépatocyte infecté, avec des inclusions intranucléaires de CMV. Des méthodes d'immunohistochimie ont révélé que la granularité basophile du cytoplasme dans les cellules sans inclusions intranucléaires classiques de CMV est due à la présence de matériel cytomégalovirus. Ainsi, non seulement les inclusions intranucléaires du virus, mais aussi la granularité basophile du cytoplasme sont un signe caractéristique de l'hépatite à CMV.
En général, chez les patients immunodéprimés, l’infection à CMV a un effet cytopathogène plus prononcé et provoque une lyse plus étendue des hépatocytes que chez les patients immunocompétents atteints d’hépatite à CMV.
Les modifications morphologiques du tissu hépatique chez les enfants atteints d'hépatite congénitale à CMV sont caractérisées par une transformation en cellules géantes des hépatocytes, une cholestase, une fibrose portale, une prolifération de l'épithélium des voies biliaires et, dans les cas de formes fulminantes, une nécrose hépatique massive.
Symptômes hépatite à cytomégalovirus
L’hépatite à cytomégalovirus peut avoir une évolution aiguë ou chronique.
 [ 23 ]
[ 23 ]
Hépatite aiguë acquise à cytomégalovirus
L'hépatite aiguë à CMV acquise chez l'enfant, l'adolescent et le jeune adulte peut être diagnostiquée dans le cadre de la mononucléose infectieuse. Cependant, dans certains cas, des lésions hépatiques isolées sont observées. La maladie se manifeste alors sous une forme anictérique, légère, modérée ou sévère. Dans des cas isolés, une hépatite fulminante peut se développer.
La période d'incubation de l'hépatite à CMV n'a pas été établie avec précision. Elle est vraisemblablement de 2 à 3 mois.
Période préictérique. Les manifestations cliniques et les paramètres biologiques de l'hépatite aiguë à CMV ne diffèrent pas fondamentalement de ceux des hépatites virales d'autres étiologies. La maladie débute progressivement. Les patients présentent une perte d'appétit, une faiblesse, des céphalées et des douleurs abdominales. Dans certains cas, la température corporelle atteint 38 °C.
La durée de la période pré-ictérique de l’hépatite A aiguë à CMV varie généralement de 3 à 7 jours.
Les manifestations cliniques de la période pré-ictérique peuvent être absentes. Dans ce cas, la forme initiale manifeste de l'hépatite à cytomégalovirus débute par l'apparition d'un ictère.
Période d'ictère. Chez les patients, après l'apparition de l'ictère, les symptômes d'intoxication observés avant l'ictère persistent, voire s'aggravent.
Les manifestations cliniques et biologiques de l’hépatite aiguë à cytomégalovirus ne sont pas fondamentalement différentes de celles de l’hépatite virale d’autres étiologies.
La durée de la période ictérique dans l’hépatite aiguë à cytomégalovirus varie de 13 à 28 jours.
La période post-ictérique de la maladie est caractérisée par une normalisation du bien-être du patient, une diminution de la taille du foie et de la rate et une diminution significative de l'activité enzymatique.
Hépatite chronique à cytomégalovirus
L'hépatite chronique à cytomégalovirus se développe le plus souvent chez les patients immunodéprimés (infectés par le VIH, recevant un traitement immunosuppresseur, ayant subi une transplantation hépatique, etc.). Ainsi, des lésions du greffon à cytomégalovirus sont observées chez 11 à 28,5 % des patients ayant subi une transplantation hépatique pour diverses raisons (maladies hépatiques auto-immunes, hépatite virale, etc.). L'ADN du CMV est détecté dans les hépatocytes de 20 % des receveurs de transplantation hépatique présentant un tableau clinique, biochimique et histologique d'hépatite.
Cependant, le développement d'une hépatite chronique à cytomégalovirus est également possible chez les enfants et les adultes immunocompétents. Dans ce cas, l'hépatite chronique peut se développer comme un processus chronique primaire ou à la suite d'une hépatite à cytomégalovirus initialement manifeste.
Les paramètres cliniques et biologiques des patients atteints d’hépatite chronique à CMV acquise ne diffèrent pas fondamentalement de ceux observés dans l’hépatite virale chronique d’autres étiologies.
Chez les patients atteints d'hépatite chronique à CMV acquise, l'activité du processus est faible à modérée. Dans près des trois quarts des cas, une fibrose hépatique modérée à sévère est diagnostiquée.
Pendant la période de rémission, les symptômes d'intoxication chez les patients atteints d'hépatite chronique acquise à CMV sont pratiquement absents. Les manifestations extrahépatiques disparaissent chez la plupart des patients. Le foie et la rate diminuent de volume, mais leur normalisation complète n'est pas observée. Habituellement, le bord du foie dépasse de 1 à 2 cm au maximum sous l'arc costal. La rate est palpée à moins de 1 cm sous le bord de l'arc costal. L'activité enzymatique sérique ne dépasse pas les valeurs normales.
Les manifestations cliniques de l'hépatite acquise à cytomégalovirus correspondent à celles d'une hépatite virale aiguë ou chronique, de gravité variable. Dans 3/4 des cas d'hépatite chronique acquise à cytomégalovirus, une fibrose hépatique modérée à sévère est diagnostiquée.
 [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ]
[ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ]
Hépatite congénitale à cytomégalovirus
L'infection congénitale à CMV peut survenir sous une forme généralisée, avec atteinte de nombreux organes et systèmes, ou sous des formes localisées, notamment hépatiques. Les lésions hépatiques sont typiques de l'infection congénitale à CMV et surviennent chez 40 à 63,3 % des patients. Les modifications hépatiques incluent l'hépatite chronique, la cirrhose, l'angiocholite et la cholestase intralobulaire. Des lésions des voies biliaires extrahépatiques, allant de l'inflammation à l'atrésie, ont été observées. À ce jour, le rôle du cytomégalovirus dans la genèse des lésions des voies biliaires extrahépatiques (atrésie, kystes) reste incertain.
L'hépatite congénitale à cytomégalovirus est observée principalement chez les enfants des premiers mois de vie. Elle évolue soit sous une forme anictérique avec hépato-splénomégalie et activité biochimique, soit sous une forme ictérique avec ictère, urines foncées, hépatosplénomégalie, hypertransaminasémie, augmentation des taux de phosphatases alcalines et de GGT, et développement d'une cirrhose hépatique chez la moitié des patients. Parallèlement, l'hépatite congénitale à cytomégalovirus peut évoluer sous des formes aiguës et prolongées avec un ictère à une ou deux vagues, des manifestations légères d'intoxication, une activité des enzymes hépatocellulaires multipliée par 2 à 3, un syndrome cholestatique (chez un tiers des patients), avec une évolution rarement chronique, qui se développe alors comme un processus chronique primaire sans ictère et avec une activité pathologique modérée à élevée.
 [ 31 ], [ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [ 37 ]
[ 31 ], [ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [ 37 ]
Hépatite chronique primaire congénitale à cytomégalovirus
Chez les enfants atteints d'hépatite chronique congénitale à CMV, une activité minimale du processus pathologique dans le foie est diagnostiquée dans 1/4 des cas, une faible activité dans 1/3 des cas et une activité modérée chez 1/3 des patients.
Le processus a une orientation fibrosante prononcée. Chez un tiers des patients, une fibrose prononcée est diagnostiquée, et chez un tiers, des signes de cirrhose du foie.
Les manifestations cliniques et les paramètres de laboratoire de l’hépatite chronique congénitale à CMV ne présentent pas de différences fondamentales par rapport à l’hépatite virale d’autres étiologies.
Pendant la période de rémission, les symptômes d'intoxication chez les patients atteints d'hépatite chronique congénitale à CMV sont pratiquement absents. Les manifestations extrahépatiques disparaissent chez la plupart des enfants. Le foie et la rate diminuent de volume, mais leur normalisation complète n'est pas observée. Habituellement, le bord du foie dépasse de 1 à 2 cm au maximum sous l'arc costal. La rate est palpée à moins de 1 cm sous le bord de l'arc costal chez la plupart des patients atteints de splénomégalie. L'activité enzymatique sérique ne dépasse pas les valeurs normales.
Hépatite à cytomégalovirus chez les patients transplantés hépatiques
L'hépatite à cytomégalovirus est la manifestation la plus fréquente de l'infection à CMV sous traitement immunosuppresseur. Dans ce cas, le diagnostic d'hépatite à cytomégalovirus est établi sur la base des résultats d'une biopsie hépatique et confirmé par culture virale, antigène ppb5, PCR et immunohistochimie. La plupart des patients atteints d'hépatite à CMV développent une atteinte hépatique isolée, et seuls quelques patients développent une infection généralisée à CMV. Du ganciclovir par voie intraveineuse est prescrit. Dans le SIDA, l'hépatite à cytomégalovirus est observée chez 3 à 5 % des patients.
Chez les patients ayant subi une transplantation hépatique orthotopique et chez les patients atteints du SIDA, des sténoses des voies biliaires extrahépatiques d'origine cytomégalovirus peuvent se développer, confirmées par la détection du virus B dans l'épithélium des voies biliaires. L'infection hépatique du donneur et du receveur par le cytomégalovirus avant la transplantation est considérée comme un facteur contribuant au rejet du greffon.
 [ 41 ], [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ]
[ 41 ], [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ]
L'évolution de l'hépatite à cytomégalovirus
L'évolution de la maladie peut être aiguë (35 %) et se terminer par une guérison avec restauration complète de l'état fonctionnel du foie en 1 à 3 mois. Chez 65 % des patients, suite à une hépatite à cytomégalovirus manifeste, la maladie devient chronique.
Où est-ce que ça fait mal?
Diagnostics hépatite à cytomégalovirus
Le diagnostic d'hépatite à cytomégalovirus repose sur une combinaison de données cliniques, biochimiques et sérologiques. La maladie débute généralement par des manifestations asthéno-dyspeptiques: malaise, faiblesse, perte d'appétit, accompagnées d'une augmentation du volume du foie et d'une hyperfermentémie. Les antécédents du patient peuvent indiquer des manipulations parentérales 2 à 3 mois avant la maladie actuelle, et le sérum sanguin ne présente aucun marqueur des virus de l'hépatite A, B, C, U, G, etc.
Il est important de noter que l'hépatite à cytomégalovirus se caractérise par un syndrome de cytolyse prononcé. Pour son indication, la détermination de l'activité des aminotransférases (ALAT, ASAT) et des fractions LDH (LDH-4, LDH-5) est largement utilisée. Une augmentation de l'activité des enzymes hépatiques est caractéristique de l'hépatite aiguë et de la phase d'exacerbation de l'hépatite chronique à cytomégalovirus. Le degré d'augmentation de l'activité des enzymes hépatiques dans diverses formes d'hépatite à cytomégalovirus correspond à celui des hépatites virales d'autres étiologies.
En présence d’ictère, il est important de déterminer le taux de bilirubine totale et le rapport des fractions conjuguées et non conjuguées.
L'activité du processus inflammatoire hépatique se reflète dans une certaine mesure dans le spectre protéique du sérum sanguin. Dans la plupart des cas, les patients atteints d'hépatite chronique à CMV présentent un taux normal de protéines sériques totales, compris entre 65 et 80 g/l. Chez les patients atteints d'hépatite chronique à CMV de forte activité, une dysprotéinémie se forme en raison d'une diminution du taux d'albumine et d'une augmentation de la fraction de globules Y et de novae. La dysprotéinémie est modérée et n'atteint une expression significative que chez certains patients, lorsque le taux d'albumine tombe en dessous de 45 % et que le taux de globuline Y dépasse 25 %.
Lors d'une exacerbation d'une hépatite chronique à cytomégalovirus, la diminution de la fonction protéique est d'autant plus importante que le processus inflammatoire hépatique est sévère. Des troubles de la coagulation sanguine (hypocoagulation) à des degrés divers se développent chez les patients atteints d'hépatite chronique, principalement en raison d'une diminution de la fonction protéique hépatique.
L'image échographique du foie dans l'hépatite CMV aiguë et chronique n'est pas différente de celle de l'hépatite virale d'autres étiologies.
La méthode d'échographie Doppler est utilisée pour déterminer le flux sanguin dans le système de la veine porte et la présence d'anastomoses porto-caves, ce qui permet le diagnostic de l'hypertension portale, y compris chez les patients atteints de cirrhose du foie d'étiologie cytomégalovirus.
Les études morphologiques permettent une évaluation objective de la nature du processus pathologique dans le foie, de sa direction et constituent également l'un des critères obligatoires pour l'efficacité de la thérapie.
Les résultats d'une ponction-biopsie peuvent avoir une valeur diagnostique différentielle décisive. Avec une ponction hépatique de taille suffisante, les informations morphologiques obtenues sont déterminantes pour évaluer l'activité et le degré de fibrose de l'hépatite chronique, ainsi que pour le choix de la stratégie thérapeutique.
Qu'est-ce qu'il faut examiner?
Qui contacter?
Traitement hépatite à cytomégalovirus
Les préparations de ganciclovir et d’interféron A recombinant sont utilisées pour traiter l’hépatite à cytomégalovirus.
Voici les résultats d'une étude clinique menée auprès de 85 enfants traités par Viferon pour une hépatite chronique à cytomégalovirus. Parmi eux, 31 enfants présentaient une hépatite acquise à CMV et 54 une hépatite congénitale à CMV. Chez 49 enfants, l'hépatite congénitale à cytomégalovirus était associée à des lésions du système biliaire (atrésie chez 44 enfants et kystes des voies biliaires chez 5) et à des lésions du système nerveux central chez 5.
Parmi les patients observés, il y avait 47 garçons et 38 filles. 55 enfants avaient moins d'un an, 23 avaient entre 1 et 3 ans et 7 avaient plus de 3 ans.
Pour le traitement de l'hépatite virale chronique, 45 enfants ont reçu une monothérapie par Viferon en suppositoires rectaux, 31 en association avec des immunoglobulines intraveineuses et 9 en association avec du ganciclovir. La dose d'interféron est de 5 millions/m² , 3 fois par semaine.
La durée du traitement a été de 6 mois chez 67 patients, de 9 mois chez 11 patients et de 12 mois chez 7 enfants. Les critères d'efficacité du traitement par interféron ont été déterminés conformément au consensus EUROHEP.
Le groupe témoin était composé de 43 enfants. Il comprenait 29 patients atteints d'hépatite congénitale et 14 d'hépatite chronique d'origine cytomégalovirus. Ces enfants ont reçu un traitement de base, comprenant uniquement des cholérétiques, des préparations vitaminiques et des hépatoprotecteurs.
En plus du suivi clinique et biochimique, l'activité réplicative du cytomégalovirus a été vérifiée au cours de l'évolution de la maladie.
La proportion d'enfants atteints d'hépatite chronique à CMV ayant obtenu une rémission complète sous traitement par Viferon était faible et n'atteignait pas 20 %. Cependant, le groupe d'enfants ayant bénéficié d'une certaine rémission représentait 78,8 % du nombre total d'enfants traités. Parallèlement, la rémission était absente chez près d'un quart des patients. Il convient également de noter qu'aucune rémission spontanée n'est apparue chez aucun enfant du groupe témoin au cours de la même période.
Une analyse comparative de l'efficacité du traitement par Viferon chez les enfants atteints d'hépatite CMV congénitale et acquise n'a montré aucune différence significative dans le pourcentage de rémission par rapport au traitement par Viferon. Les valeurs de p variaient de p > 0,05 à p > 0,2.
Afin de répondre à la question de la dépendance de la fréquence de rémission de l'hépatite à cytomégalovirus au cours du traitement par rapport au schéma thérapeutique, trois groupes ont été identifiés. Le premier comprenait les patients ayant reçu une monothérapie par Viferon, le deuxième les enfants ayant reçu Viferon en association avec des immunoglobulines intraveineuses, et le troisième les patients ayant reçu une thérapie combinée par Viferon et ganciclovir.
Aucune différence significative n'a été observée dans les résultats du traitement entre les patients des différents groupes. Seule une tendance à une cytolyse moins sévère a été observée chez les enfants recevant un traitement combiné par Viferon et immunoglobulines intraveineuses. Les valeurs de p variaient de p > 0,05 à p > 0,1.
Une tendance similaire est observée lors de l'évaluation de l'activité réplicative du CMV dans l'hépatite chronique à cytomégalovirus chez les enfants ayant reçu différents schémas thérapeutiques. La fréquence de détection de l'ADN du CMV lors de l'observation dynamique était pratiquement identique chez les enfants des trois groupes. Une activité réplicative du CMV légèrement inférieure a été observée chez les patients traités par Viferon en association avec des immunoglobulines intraveineuses. Les valeurs de p variaient de p > 0,05 à p > 0,2.
Plus d'informations sur le traitement
La prévention
Aucune prévention spécifique de l'infection à CMV n'a été mise au point. Des travaux expérimentaux sont en cours pour créer un vaccin.
Aucune mesure anti-épidémique n'est appliquée dans les foyers d'infection. Compte tenu du rôle potentiel du mécanisme parentéral d'infection dans la formation de l'hépatite à cytomégalovirus, des mesures visant à supprimer toute possibilité d'infection parentérale, y compris transfusionnelle, semblent particulièrement importantes. L'utilisation d'aiguilles jetables et le respect des règles de stérilisation des instruments chirurgicaux permettent de prévenir totalement l'infection lors des manipulations parentérales.
Pour prévenir l’infection par le cytomégalovirus lors des transfusions de sang et de ses composants, il est nécessaire de décider de tester le sang du donneur pour l’ADN du CMV.

