Expert médical de l'article
Nouvelles publications
Cathétérisme cardiaque
Dernière revue: 06.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
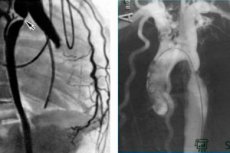
Le cathétérisme des cavités cardiaques est réalisé par ponction et insertion percutanée d'un cathéter dans un vaisseau - une veine périphérique (cubitale, sous-clavière, jugulaire, fémorale) pour les cavités droites du cœur ou une artère (brachiale, fémorale, axillaire, radiale) pour les cavités gauches du cœur.
Méthodologie de réalisation du cathétérisme cardiaque
En cas de rétrécissement sévère de la valve aortique ou de sa prothèse artificielle, lorsqu'il est impossible de passer rétrogradement un cathéter dans le ventricule gauche, une ponction transseptale du septum interauriculaire, de l'oreillette droite vers l'oreillette gauche, puis dans le ventricule gauche, est réalisée. L'approche vasculaire la plus fréquemment utilisée est la méthode de Seldinger (1953). Après anesthésie locale de la peau et du tissu sous-cutané avec une solution de novocaïne à 0,5-1 % ou de lidocaïne à 2 %, et une petite incision cutanée, une veine ou une artère est ponctionnée à l'aide d'une aiguille. Lorsque du sang apparaît à l'extrémité proximale de l'aiguille (pavillon) (il est nécessaire de tenter de ne ponctionner que la paroi antérieure du vaisseau), un fil-guide est inséré dans l'aiguille, celle-ci est retirée et un cathéter est introduit dans le vaisseau le long du fil-guide, qui, bien entendu, doit être plus long que le cathéter. Le cathéter est avancé jusqu'à l'emplacement souhaité sous contrôle radiologique. En cas d'utilisation de cathéters flottants de type Swan-Gans avec ballonnet à l'extrémité, l'emplacement de l'extrémité du cathéter est déterminé par la courbe de pression. Il est préférable d'installer un introducteur à paroi mince, muni d'une valve hémostatique et d'une branche latérale pour le lavage vasculaire. Grâce à celui-ci, le cathéter peut être facilement inséré et remplacé si nécessaire. Le cathéter et l'introducteur sont lavés avec une solution isotonique de chlorure de sodium héparinée afin de prévenir la formation de thrombus. Différents types de cathéters permettent d'atteindre différentes parties du cœur et des vaisseaux, d'y mesurer la pression, de prélever des échantillons de sang pour oxymétrie et autres examens, et d'introduire la veine cave supérieure (VCR) afin de déterminer les paramètres anatomiques, les constrictions, les écoulements sanguins, etc.
En l'absence de contrôle radioscopique (radiographique) de l'emplacement du cathéter, on utilise des cathéters munis d'un ballonnet flottant gonflable à leur extrémité. Ce dernier peut se déplacer avec le flux sanguin vers l'oreillette droite, le ventricule droit et l'artère pulmonaire, et enregistrer la pression à l'intérieur de ces derniers. La pression artérielle pulmonaire permet d'évaluer indirectement l'état de la fonction ventriculaire gauche, sa pression télédiastolique (PTD), puisque la PTD ventriculaire gauche correspond à la pression moyenne dans l'oreillette gauche ou dans les capillaires pulmonaires. Ceci est important pour le suivi thérapeutique en cas d'hypotension, d'insuffisance cardiaque, par exemple en cas d'infarctus aigu du myocarde. Si le cathéter est équipé de dispositifs supplémentaires, il est possible de mesurer le débit cardiaque par dilution de colorant ou thermodilution, d'enregistrer un électrogramme intracavitaire et de réaliser une stimulation endocardique. Les courbes de pression intracavitaire sont enregistrées à l'aide d'un capteur de pression liquide Statham et d'un ECG sur un enregistreur à jet ou un ordinateur, avec possibilité d'impression sur papier. leurs changements peuvent être utilisés pour juger une pathologie cardiaque particulière.
Mesure du débit cardiaque
Il convient de noter qu'il n'existe pas de méthode absolument précise pour mesurer le débit cardiaque. Lors d'un cathétérisme cardiaque, trois méthodes sont le plus souvent utilisées: la méthode de Fick, la méthode de thermodilution et la méthode angiographique.
La méthode de Fick
Proposée par Adolph Fick en 1870, cette méthode repose sur l'hypothèse qu'au repos, l'apport d'oxygène aux poumons est égal à la quantité d'oxygène utilisée par les tissus, et que la quantité de sang éjecté par le ventricule gauche est égale au volume sanguin circulant dans les poumons. Le prélèvement de sang veineux mixte est indispensable, car la concentration en oxygène dans le sang de la veine cave et du sinus coronaire diffère significativement. Le prélèvement sanguin est privilégié dans le VD ou l'artère pulmonaire. La différence artérioveineuse en oxygène peut être déterminée à partir de la concentration en oxygène dans le sang artériel (Ca) et veineux (Cv). En calculant la teneur en oxygène absorbée pendant une minute, on peut calculer le volume sanguin circulant dans les poumons pendant la même période, c'est-à-dire le débit cardiaque (DC):
MO = Q / Ca - St (l/min),
Où Q est l'absorption d'oxygène par le corps (ml/min).
Connaissant l'index cardiaque, vous pouvez calculer l'indice cardiaque (IC). Pour ce faire, divisez l'index cardiaque par la surface de gel du patient, calculée en fonction de sa taille et de son poids. Chez un adulte, l'index cardiaque est normalement de 5 à 6 l/min et l'IC de 2,8 à 3,5 l/min/ m².
Méthode de thermodilution
Cette méthode utilise une solution isotonique refroidie de chlorure de sodium (5 à 10 ml), introduite dans l'oreillette droite par un cathéter multilumière. L'extrémité du cathéter munie de la thermistance est insérée dans l'artère pulmonaire. L'étalonnage des courbes s'effectue par l'activation brève d'une résistance constante, ce qui permet d'obtenir les écarts de l'enregistreur correspondant à une variation de température pour une thermistance donnée. La plupart des appareils de thermodilution sont équipés de calculateurs analogiques. Les équipements modernes permettent d'effectuer jusqu'à trois mesures de la MO sanguine en une minute et de répéter les études à plusieurs reprises. Le débit cardiaque, ou MO, est déterminé par la formule suivante: MO = V (T1 - T2) x 60 x 1,08 / S (l/min).
Où V est le volume de l'indicateur introduit; T1 est la température du sang; T2 est la température de l'indicateur; S est l'aire sous la courbe de dilution; 1,08 est le coefficient dépendant de la densité spécifique et de la capacité thermique du sang et de la solution isotonique de chlorure de sodium.
Les avantages de la thermodilution, ainsi que la nécessité de cathétériser uniquement le lit veineux, font de cette méthode actuellement la plus acceptable pour déterminer le débit cardiaque en pratique clinique.
Quelques aspects techniques du laboratoire de cathétérisme
Le personnel du laboratoire d'angiographie par cathétérisme comprend le chef, les médecins, les infirmiers et les techniciens en radiologie (techniciens en radiologie) si des films cinématographiques et radiographiques grand format sont utilisés. Dans les laboratoires utilisant uniquement des films vidéo et des images numériques, la présence de techniciens en radiologie n'est pas nécessaire. L'ensemble du personnel du laboratoire doit maîtriser les techniques de réanimation cardio-pulmonaire, pour lesquelles le bloc opératoire radiologique doit être équipé des médicaments appropriés, d'un défibrillateur, d'un appareil de stimulation cardiaque électrique avec un jeu de cathéters à électrodes, d'une alimentation centrale en oxygène et (de préférence) d'un appareil de ventilation artificielle.
Les interventions diagnostiques complexes et risquées, ainsi que les ICP (angioplastie, pose de stent, athérectomie, etc.), doivent de préférence être réalisées dans des cliniques disposant d'une équipe de chirurgie cardiaque. Selon les recommandations de l'American College of Cardiology/American Heart Association, l'angioplastie et l'examen des patients présentant un risque élevé de complications (IDM) peuvent être réalisés par des spécialistes expérimentés et qualifiés sans la présence d'un chirurgien cardiaque à l'hôpital, si le patient ne peut être transporté vers un lieu plus adapté sans risque supplémentaire. En Europe et dans certains autres pays (dont la Russie), les interventions endovasculaires sont de plus en plus souvent réalisées sans la présence de chirurgiens cardiaques, le recours à une chirurgie cardiaque d'urgence étant actuellement extrêmement faible. Un accord avec une clinique de chirurgie cardiovasculaire proche suffit pour y transférer le patient en urgence en cas de complications péri- et post-interventionnelles.
Afin de maintenir la forme, la qualification et les compétences des opérateurs, le laboratoire doit réaliser au moins 300 interventions par an, et chaque médecin au moins 150 interventions diagnostiques par an. Pour le cathétérisme et l'angiographie, un appareil d'angiographie à rayons X haute résolution, un système de surveillance de l'ECG et de la pression intravasculaire, d'archivage et de traitement des images angiographiques, des instruments stériles et divers types de cathéters sont nécessaires (les différents types de cathéters pour l'angiographie coronaire sont décrits ci-dessous). L'appareil d'angiographie doit être équipé d'un dispositif d'acquisition et d'archivage d'images cinéangiographiques ou numériques, et permettre l'acquisition d'images en ligne, c'est-à-dire immédiatement avec analyse quantitative informatique des angiogrammes.
Modifications des courbes de pression intracavitaire
Les courbes de pression intracavitaire peuvent varier selon les pathologies. Ces modifications servent au diagnostic lors de l'examen des patients atteints de diverses pathologies cardiaques.
Pour comprendre les causes des variations de pression dans les cavités cardiaques, il est nécessaire de comprendre les relations temporelles entre les processus mécaniques et électriques intervenant au cours du cycle cardiaque. L'amplitude de l'onde a dans l'oreillette droite est supérieure à celle de l'onde Y. Un excès de l'onde Y sur l'onde a dans la courbe de pression de l'oreillette droite indique un défaut de remplissage de l'oreillette pendant la systole ventriculaire, ce qui se produit en cas d'insuffisance ou de malformation de la valve tricuspide.
En cas de sténose tricuspide, la courbe de pression auriculaire droite ressemble à celle de l'oreillette gauche en cas de sténose mitrale ou de péricardite constrictive, avec une baisse et un plateau en milieu et fin de diastole, caractéristiques des pressions élevées en début de systole. La pression auriculaire gauche moyenne correspond assez étroitement à la pression artérielle pulmonaire bloquée et à la pression diastolique du tronc pulmonaire. En cas d'insuffisance mitrale sans sténose, on observe une baisse rapide de la pression au début de la systole (diminution de l'onde Y), suivie d'une augmentation progressive en fin de diastole (diastasis). Ceci reflète l'équilibre entre les pressions auriculaire et ventriculaire atteint pendant la phase tardive du remplissage ventriculaire. En revanche, chez les patients présentant une sténose mitrale, l'onde Y diminue lentement, tandis que la pression dans l'oreillette gauche continue de diminuer tout au long de la diastole. Il n'y a aucun signe de diastasis de la pression différentielle dans l'oreillette gauche, le gradient de pression auriculo-ventriculaire étant préservé. Si la sténose mitrale s'accompagne d'un rythme sinusal normal, l'onde α de l'oreillette gauche est préservée et la contraction des oreillettes crée un important gradient de pression. Chez les patients présentant une insuffisance mitrale isolée, l'onde V est clairement exprimée et présente un coude descendant prononcé de la ligne Y.
Sur la courbe de pression ventriculaire gauche, le point de pression expiratoire (PED) précède immédiatement le début de sa contraction isométrique et se situe immédiatement après l'onde a, précédant l'onde c de la pression auriculaire gauche. La PED ventriculaire gauche peut augmenter dans les cas suivants: insuffisance cardiaque, si le ventricule subit une charge importante causée par un débit sanguin excessif, par exemple en cas d'insuffisance aortique ou mitrale; hypertrophie ventriculaire gauche, accompagnée d'une diminution de sa distensibilité, de son élasticité et de sa compliance; cardiomyopathie restrictive; péricardite constrictive; tamponnade cardiaque causée par un épanchement péricardique.
En cas de sténose valvulaire aortique, qui s'accompagne d'une obstruction du flux sanguin du ventricule gauche et d'une augmentation de la pression aortique par rapport à la pression systolique (apparition d'un gradient de pression), la courbe de pression ventriculaire gauche ressemble à celle observée lors d'une contraction isométrique. Ses contours sont plus symétriques et la pression maximale apparaît plus tardivement que chez les personnes en bonne santé. Un tableau similaire est observé lors de l'enregistrement de la pression ventriculaire droite chez les patients atteints de sténose de l'artère pulmonaire. Les courbes de pression artérielle peuvent également différer selon le type de sténose aortique. Ainsi, en cas de sténose valvulaire, on observe une augmentation lente et retardée de l'onde de pouls artérielle, tandis qu'en cas de cardiomyopathie hypertrophique, la forte augmentation initiale de la pression est remplacée par une diminution rapide, puis par une onde positive secondaire reflétant l'obstruction pendant la systole.
Indices dérivés de la pression intraventriculaire
La vitesse de variation/augmentation de la courbe de pression intraventriculaire pendant la phase de contraction isovolumique est appelée dérivée première – dр/dt. Auparavant, elle était utilisée pour évaluer la contractilité du myocarde ventriculaire. La valeur de dр/dt et la dérivée seconde – dр/dt/р – sont calculées à partir de la courbe de pression intraventriculaire à l'aide de techniques électroniques et informatiques. Les valeurs maximales de ces indicateurs représentent les indices de la fréquence de contraction ventriculaire et permettent d'évaluer la contractilité et l'état inotrope du cœur. Malheureusement, la large gamme de ces indicateurs chez différentes catégories de patients ne permet pas d'établir de normes moyennes, mais ils sont tout à fait applicables chez un patient donné, avec des données initiales et dans le contexte de l'utilisation de médicaments améliorant la fonction contractile du muscle cardiaque.
Actuellement, disposant dans notre arsenal de méthodes d'examen des patients telles que l'échocardiographie dans ses diverses modifications, l'imagerie par ordinateur (CT), le faisceau d'électrons et l'imagerie par résonance magnétique (IRM), ces indicateurs pour le diagnostic des pathologies cardiaques ne sont plus aussi importants qu'avant.
Complications du cathétérisme cardiaque
Le cathétérisme cardiaque est relativement sûr. Cependant, comme toute technique invasive, il présente un certain pourcentage de complications liées à l'intervention elle-même et à l'état général du patient. L'utilisation de cathéters atraumatiques plus avancés et plus fins, de RVS à faible osmolarité et/ou non ionique, et d'unités angiographiques modernes avec traitement d'images par ordinateur en temps réel pour les interventions invasives a considérablement réduit l'incidence des complications possibles. Ainsi, la mortalité lors d'un cathétérisme cardiaque dans les grands laboratoires d'angiographie ne dépasse pas 0,1 %. S. Pepine et al. rapportent un taux de mortalité global allant jusqu'à 0,14 %, avec 1,75 % pour les patients de moins d'un an, 0,25 % pour les personnes de plus de 60 ans, 0,03 % pour les coronaropathies monovasculaires, 0,16 % pour les coronaropathies trivasculaires et 0,86 % pour les coronaropathies gauches. En cas d'insuffisance cardiaque, la mortalité augmente également en fonction de la classe NUHA: en FC I-II - 0,02 %, FC III et IV - 0,12 et 0,67 %, respectivement. Chez certains patients, le risque de complications graves est accru. Il s'agit de patients présentant une angine instable et progressive, un infarctus du myocarde récent (moins de 7 jours), des signes d'œdème pulmonaire dû à une ischémie myocardique, une insuffisance circulatoire de FC III-IV, une insuffisance ventriculaire droite sévère, des malformations cardiaques valvulaires (sténose aortique sévère et régurgitation aortique avec une pression différentielle supérieure à 80 mm Hg), des malformations cardiaques congénitales avec hypertension pulmonaire et insuffisance ventriculaire droite.
Dans une analyse multivariée portant sur 58 332 patients, les facteurs prédictifs de complications graves étaient l'insuffisance cardiaque congestive sévère, l'hypertension, la cardiopathie congénitale, la valvulopathie aortique et mitrale, l'insuffisance rénale, l'angor instable et l'infarctus aigu du myocarde dans les 24 premières heures, ainsi que la cardiomyopathie. Chez les patients de 80 ans, la mortalité lors des procédures diagnostiques invasives a également augmenté à 0,8 %, et l'incidence des complications vasculaires au site de ponction a atteint 5 %.


 [
[