Expert médical de l'article
Nouvelles publications
Diagnostic des stades du cancer de la prostate
Dernière revue: 04.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
Cliniquement, une distinction est faite entre le cancer localisé (T 1-2, N 0, M 0 ), localement avancé (T 3-4, N 0-1, M 0 ) et généralisé (T 1-4, N 0-1, M 1 ).
Les patients présentant des stades cliniquement localisés et localement avancés sont classés selon le degré de risque (D'Amico A V. et al., 2003):
- faible: stade T 1a-c; taux de PSA inférieur à 10 ig/ml: classification de Gleason - 2-5; en biopsie - lésion unilatérale inférieure à 50 %:
- modéré: stade T 2a; taux de PSA inférieur à 10 ng/ml; score de Gleason - 3 + 4 = 7; à la biopsie - lésion bilatérale inférieure à 50 %;
- stade élevé T 2b, T 3a-b; taux de PSA - 10-20 ng/ml; classification de Gleason - plus de 4 + 3 - 7; à la biopsie - lésions supérieures à 50 %, invasion périnerveuse;
- très élevé: stade T 4; taux de PSA supérieur à 20 ng/ml; score de Gleason supérieur à 8; la biopsie montre une invasion lymphovasculaire.
Une fois le diagnostic établi et l'étendue du processus établie (localisée, localement avancée ou généralisée), le médecin et le patient doivent choisir la méthode de traitement. Dans la société moderne, une grande importance est accordée à la qualité de vie des patients après le début du traitement. La qualité de vie sans traitement correspond à l'évolution de la maladie sous-jacente et dépend de la progression du processus oncologique. Les altérations de la qualité de vie surviennent principalement après le début du traitement et le recours à une méthode thérapeutique ou chirurgicale. Établir clairement le stade du processus permet non seulement de choisir la méthode de traitement optimale, mais aussi de prédire l'évolution ultérieure de la maladie.
La détermination du taux de PSA, associée au tableau clinique du cancer de la prostate et à la gradation de la tumeur selon l'échelle de Gleason, augmente significativement la valeur informative de chacun des indicateurs cités pour établir le stade pathologique du cancer. AV Partin et al. (1997) ont proposé des tableaux pronostiques permettant de prédire la propagation tumorale, le choix de la méthode de traitement, le degré de radicalité et le pronostic de l'efficacité du traitement.
Pour évaluer l'extension tumorale, les méthodes les plus couramment utilisées sont le toucher rectal, l'échographie transrectale, la détermination du taux de PSA et la scintigraphie osseuse. Si nécessaire, une tomodensitométrie (TDM) ou une imagerie par résonance magnétique (IRM) et une radiographie pulmonaire sont prescrites.
Toutes les méthodes d'imagerie visent à déterminer le stade et à évaluer l'efficacité du traitement. Après avoir confirmé le diagnostic, l'urologue doit préciser le volume de la tumeur primitive, ses limites et son potentiel invasif ou métastatique. Tous ces indicateurs sont essentiels pour le pronostic de la maladie et le choix du traitement.
Tumeur primaire (T)
Tout d'abord, il est nécessaire de déterminer si la tumeur est limitée à la prostate (T 1-2 ) ou s'étend au-delà de la capsule (T 3-4 ). L'examen digital ne permet souvent pas d'évaluer l'extension tumorale. Selon certaines données, les résultats du toucher rectal correspondent à ceux de l'examen histologique chez moins de 50 % des patients. Cependant, un examen plus approfondi n'est indiqué que pour décider d'un traitement radical.
Le taux de PSA peut refléter l'étendue de la tumeur, mais ne permet pas de déterminer précisément le stade morphologique. La combinaison du taux de PSA, de l'indice de Gleason et des données de palpation permet une meilleure prédiction du stade morphologique que chacun de ces paramètres pris séparément. La valeur du PSA libre est controversée: dans une étude, la détermination du taux de PSA libre a permis de préciser le stade des tumeurs localisées, mais d'autres études ne l'ont pas confirmé. Seules des études approfondies permettront de résoudre ce problème.
L'échographie transrectale est le plus souvent utilisée pour examiner l'état de la prostate. Cette méthode ne détecte que 60 % des tumeurs et ne montre pas toujours d'invasion capsulaire. Près de 60 % des patients présentent un stade T3 . L'échographie révèle un processus moins fréquent. Les signes échographiques d'invasion capsulaire sont un renflement, une irrégularité et une rupture du contour de la glande. L'invasion des vésicules séminales par des cellules tumorales est un signe de mauvais pronostic, mais les informations la concernant sont extrêmement importantes pour le choix d'une méthode de traitement. Lors de la réalisation d'une échographie transrectale, il convient de prêter attention à l'échostructure des vésicules (hyperéchogénicité), à leur asymétrie, à leur déformation et à leur expansion. De plus, une lésion des vésicules séminales est indiquée par une perte de rondeur et une compaction à la base de la glande. Ces signes étant assez subjectifs, il est inapproprié de se fier entièrement aux données échographiques. L'invasion des vésicules séminales indique un risque élevé de récidive locale et de métastases, et leur biopsie est indiquée pour clarifier le diagnostic (avant intervention chirurgicale). L'examen ne doit pas débuter par cette procédure, mais si le risque d'invasion est élevé et que le choix du traitement dépend du résultat de la biopsie, sa mise en œuvre est justifiée. Un résultat négatif n'exclut pas une invasion microscopique. En règle générale, une biopsie des vésicules séminales est réalisée au stade clinique T 2b et plus et si le taux de PSA est supérieur à 10 ng/ml. Le résultat est considéré comme positif si au moins une biopsie de la base de la prostate contient des cellules tumorales. Outre des examens complémentaires, une analyse approfondie des résultats de la biopsie primaire permet d'améliorer la précision de la détermination clinique du stade (le nombre et l'étendue des foyers tumoraux, ainsi que l'invasion capsulaire jouent un rôle). Le degré de différenciation est également important: avec un indice de Gleason inférieur à 6, la tumeur est localisée dans 70 % des cas.
Le flux sanguin dans la prostate cancéreuse est plus élevé que dans une glande normale ou hyperplasique. Après castration, l'intensité du flux sanguin dans la glande diminue. Le développement de cartes écho-Dopplerographiques pour le diagnostic et le suivi du cancer de la prostate est prometteur, mais il n'existe actuellement aucune donnée fiable sur son utilisation pour déterminer le stade du processus local. Cette méthode permet d'obtenir du matériel supplémentaire lors d'une biopsie ciblée à partir de foyers de vascularisation pathologique.
Les résultats de la visualisation du cancer de la prostate dépendent directement de l'équipement technique de la clinique et de l'expérience du spécialiste. C'est pourquoi toutes les méthodes de visualisation modernes jouent un rôle non pas déterminant, mais éclairant, et le choix de la méthode de traitement repose sur une combinaison de données d'examen clinique et d'études instrumentales.
L'IRM offre les meilleures capacités pour visualiser la structure de la prostate. La norme moderne pour l'examen des organes pelviens par IRM est l'utilisation d'un capteur endorectal, qui permet d'obtenir une image avec une résolution spatiale maximale de 0,5 à 1 mm. L'introduction d'air dans le capteur endorectal permet une visualisation claire de la capsule prostatique, des angles rectoprostatiques et du fascia rectoprostatique de Denonvilliers. L'utilisation d'un capteur endorectal en IRM ne limite pas la visualisation des ganglions lymphatiques régionaux (jusqu'au niveau de la bifurcation de l'aorte abdominale). Le cancer de la prostate se caractérise par un faible signal sur les images pondérées en T, sur fond d'un signal élevé provenant d'une zone périphérique inchangée de la prostate. Une forme irrégulière, une propagation diffuse avec effet de masse, des contours flous et irréguliers sont des caractéristiques morphologiques des foyers de faible signal dans la zone périphérique de la prostate, suggérant une nature néoplasique de la lésion. Lors de la réalisation d'un contraste dynamique, les foyers cancéreux accumulent rapidement le produit de contraste au temps artériel et l'éliminent rapidement, ce qui reflète le degré d'angiogenèse et, par conséquent, le degré de malignité de la tumeur. Une faible intensité du signal est également caractéristique des foyers d'hémorragies post-biopsie, de prostatite, d'hyperplasie stromale bénigne de la zone neutre de la glande, de modifications fibro-cicatricielles, d'hyperplasie fibromusculaire, et des conséquences d'une hormonothérapie ou d'une radiothérapie. L'IRM sans contraste dynamique ne permet pas de différencier de manière fiable la plupart de ces modifications et maladies.
Comme indiqué précédemment, l'une des principales tâches de toute méthode d'imagerie pour le cancer de la prostate est de déterminer le volume de la lésion glandulaire et la propagation de la tumeur au-delà de la capsule. La détermination du volume tumoral est importante pour le pronostic. Un volume tumoral inférieur à 4 cm³ indique des métastases à distance, et 12 cm³ indique une probabilité extrêmement élevée de métastases. Selon les recherches, la précision de l'IRM pour détecter les foyers de lésions néoplasiques de la prostate varie de 50 à 90 %. La sensibilité de l'IRM pour déterminer la localisation du cancer de la prostate est d'environ 70 à 80 %, tandis que les foyers microscopiques de cancer (foyers) ne peuvent pas être détectés par IRM.
L'avantage principal de l'IRM endorectale est sa capacité à localiser des lésions néoplasiques dans des zones inaccessibles aux autres méthodes diagnostiques et à préciser la nature et la direction de la croissance tumorale. Par exemple, l'IRM permet de détecter des lésions néoplasiques dans les parties antérieures de la zone périphérique de la prostate, inaccessibles par biopsie transrectale. En général, l'IRM complète significativement les données du toucher rectal et de l'échographie transrectale sur la localisation tumorale.
L'IRM endorectale permet de visualiser la capsule glandulaire, les faisceaux vasculo-nerveux, les vésicules séminales, l'apex glandulaire et le plexus veineux périprostatique, ainsi que de déterminer la prévalence locale de la tumeur glandulaire. Il convient de souligner que la pénétration de la capsule est considérée comme un signe microscopique, et même les appareils d'IRM modernes (antenne endorectale) ne sont pas en mesure de fournir de telles informations. Seules les données sur la croissance au-delà de la capsule glandulaire sont obtenues.
Critères diagnostiques de l'extension extracapsulaire par IRM:
- la présence d’une tumeur extracapsulaire;
- contour irrégulier de la glande (déformation, angularité);
- asymétrie des faisceaux neurovasculaires;
- oblitération des angles rectoprostatiques;
- contact large de la tumeur avec la capsule.
La spécificité et la précision maximales (jusqu'à 95-98 %) des résultats d'IRM sont obtenues lors de l'examen des patients présentant un risque moyen ou élevé d'invasion extracapsulaire. L'invasion extracapsulaire (selon les données de l'IRM) est considérée comme un indicateur de l'inadéquation du traitement chirurgical et d'un pronostic défavorable. L'hormonothérapie ou la radiothérapie n'affectent pas la précision de la détection de la propagation extracapsulaire d'une tumeur prostatique. La principale difficulté pour détecter les foyers cancéreux et la propagation extracapsulaire d'une tumeur réside dans la grande variabilité de l'interprétation des tomogrammes par les différents spécialistes. La principale tâche d'un spécialiste en radiodiagnostic est d'obtenir une spécificité diagnostique élevée (même au détriment de la sensibilité) afin de ne pas priver les patients opérables de la possibilité d'un traitement radical.
La similarité de densité des tissus prostatiques cancéreux, hyperplasiques et normaux en TDM rend cette méthode peu utile pour évaluer la propagation locale de la tumeur. L'invasion des vésicules séminales est plus importante que celle des capsules, mais même dans ce cas, la TDM n'apporte d'informations que dans les cas avancés. Cependant, cette méthode est activement utilisée pour marquer la zone d'impact avant la radiothérapie.
La lenteur du développement du diagnostic radiologique dans notre pays a entraîné un diagnostic tardif du cancer de la prostate et, par conséquent, une prévalence insuffisante des méthodes radicales de traitement du cancer de la prostate (par exemple, la prostatectomie), une faible disponibilité des tomographes modernes et l'absence de programmes de formation appropriés pour les spécialistes en diagnostic radiologique et les urologues. Malgré la généralisation de la tomodensitométrie et de l'IRM, le niveau d'équipement des cabinets et la formation des spécialistes en diagnostic radiologique sont insuffisants pour que les informations obtenues soient déterminantes dans le choix d'une méthode de traitement pour les patients atteints d'un cancer de la prostate.
Ganglions lymphatiques régionaux (N)
Les ganglions lymphatiques régionaux ne doivent être évalués que lorsque cela affecte directement la stratégie thérapeutique (généralement lors de la planification d'un traitement radical). Un taux élevé de PSA, des tumeurs T2c -T3a, une faible différenciation et une invasion périneurale sont associés à un risque élevé de métastases ganglionnaires. L'évaluation de l'état ganglionnaire par le taux de PSA est jugée insuffisante.
Seule la lymphadénectomie (ouverte ou laparoscopique) fournit les informations nécessaires. Des études récentes sur la lymphadénectomie étendue ont montré que le cancer de la prostate n'affecte pas toujours les ganglions obturateurs. En cas de tumeurs asymptomatiques et de taux de PSA inférieurs à 20 kg/ml, la TDM ne confirme l'hypertrophie ganglionnaire que dans 1 % des cas. Le recours à l'IRM ou à la TDM est justifié en cas de risque élevé de métastases, la spécificité de ces méthodes atteignant 93 à 96 %. Cependant, même un résultat positif peut être erroné, et seule la ponction d'un ganglion suspect permet de refuser la lymphadénectomie. Selon une analyse rétrospective, la taille du ganglion n'indique pas toujours la présence de métastases; l'asymétrie des ganglions affectés est considérée comme un signe plus révélateur. Actuellement, seuls 2 à 3 % des patients ayant subi une prostatectomie radicale pour un cancer de la prostate localisé reçoivent un diagnostic de métastases ganglionnaires sur la base d'un examen histologique postopératoire.
La tomographie par émission de positons (TEP) et la scintigraphie avec anticorps marqués sont recommandées comme méthodes de détection des métastases dans les ganglions lymphatiques, mais leur utilisation est encore limitée en raison d'une sensibilité insuffisante.
Les nomogrammes de Partin (2001) permettent d'évaluer le risque d'envahissement ganglionnaire régional. Ces nomogrammes sont des algorithmes mathématiques utilisés pour un patient ou un groupe de patients. Ces tables permettent de déterminer la probabilité d'extension tumorale locale (capsule, vésicules séminales) et d'envahissement ganglionnaire en fonction du stade clinique, du taux de PSA et de l'indice de Gleason. Ils permettent notamment d'identifier un groupe de patients présentant une faible probabilité (moins de 10 %) de métastases ganglionnaires (avec un taux de PSA supérieur à 20 ng/mj, un stade T 1-2a et un indice de Gleason compris entre 2 et 6); dans ce groupe, l'état ganglionnaire peut ne pas être précisé avant un traitement radical. Le risque de métastases ganglionnaires peut également être évalué en détectant les zones tumorales présentant une anaplasie prononcée (4-5 points): si ces zones sont retrouvées sur quatre biopsies ou plus, ou si elles prédominent sur au moins une biopsie, le risque atteint 20-45 %. Chez d'autres patients, ce taux ne dépasse pas 2,5 %. Aucun examen complémentaire n'est alors nécessaire.
Métastases à distance (M)
Chez 85 % des patients décédant d'un cancer de la prostate, des lésions du squelette axial sont détectées. Les métastases osseuses surviennent suite à la pénétration de cellules cancéreuses dans la moelle osseuse par la circulation sanguine, ce qui entraîne la croissance tumorale et la lyse des structures osseuses. La prévalence des métastases osseuses influence le pronostic, et leur détection précoce alerte le médecin sur d'éventuelles complications. Dans 70 % des cas, les métastases s'accompagnent d'une augmentation de l'activité de l'isoenzyme osseuse de la phosphatase alcaline (ALP). La détermination de l'activité de l'ALP et du taux de PSA permet dans la grande majorité des cas de détecter des métastases osseuses. Selon l'analyse multivariée, ces indicateurs ne sont affectés que par le nombre de métastases osseuses. Il est important que l'activité de l'isoenzyme osseuse de l'ALP reflète l'étendue des lésions osseuses plus précisément que le taux de PSA.
La scintigraphie est considérée comme la méthode la plus sensible pour détecter les métastases osseuses (supérieure à la radiographie et à la détermination de l'activité des phosphatases alcalines et acides). Les diphosphonates de technétium sont plus indiqués comme radiopharmaceutiques, car leur accumulation dans les os est beaucoup plus importante que dans les tissus mous. Une corrélation a été démontrée entre l'évaluation semi-quantitative des lésions osseuses et la survie. La détection de métastases à distance est possible dans n'importe quel organe. Elles surviennent le plus souvent dans les ganglions lymphatiques non régionaux, les poumons, le foie, le cerveau et la peau. En cas de symptômes correspondants, la radiographie pulmonaire, l'échographie, le scanner et l'IRM sont utilisés pour les détecter. Les tactiques en cas de suspicion de métastases osseuses sont présentées dans le schéma.
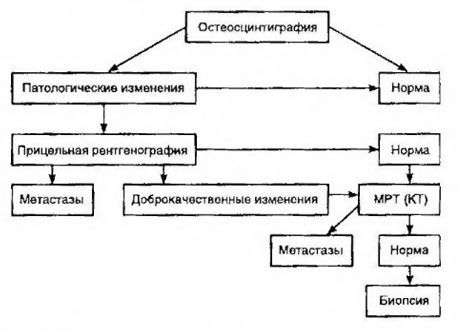
L'indicateur biologique le plus fiable pour déterminer le degré de métastase est le taux de PSA. Il a été démontré qu'une augmentation de plus de 100 ng/ml est le seul paramètre permettant d'indiquer de manière fiable la présence de métastases à distance. La détermination du taux de PSA réduit le nombre de patients nécessitant une scintigraphie osseuse. La probabilité de détecter des métastases osseuses avec une diminution du taux de PSA est très faible. En l'absence de symptômes et avec un taux initial de PSA inférieur à 20 ng/ml, la scintigraphie permet de détecter des tumeurs hautement et moyennement différenciées. En revanche, en cas de tumeurs peu différenciées et d'invasion capsulaire, la scintigraphie est indiquée (quel que soit le taux de PSA).


 [
[