Expert médical de l'article
Nouvelles publications
Pathogenèse de l'hépatite B
Dernière revue: 19.11.2021

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
Dans la pathogenèse de l'hépatite B, plusieurs liens principaux de la chaîne pathogénique peuvent être distingués:
- introduction de l'agent pathogène - infection;
- fixation sur l'hépatocyte et pénétration dans la cellule;
- multiplication du virus et "poussée" sur la surface de l'hépatocyte, et aussi dans le sang;
- l'inclusion de réactions immunologiques visant à éliminer le pathogène;
- lésion immunocomplexe des organes et des systèmes;
- formation de l'immunité, libération de l'agent pathogène, récupération.
Comme l'infection par l'hépatite B survient toujours par voie parentérale, on peut supposer que le moment de l'infection est presque équivalent à la pénétration du virus dans le sang. Les tentatives de certains chercheurs d'isoler dans la phase entérale et régionale de l'hépatite B sont mal fondées. Il y a plus de raisons de croire qu'avec la circulation sanguine, le virus pénètre immédiatement dans le foie.
Tropisme du virus de l'hépatite B au tissu hépatique est prédéterminée par la présence dans l'HBsAg d'un récepteur spécial - un polypeptide avec un poids moléculaire de 31 000 Da (RZ1), qui a une activité de liaison à l'albumine. Une zone similaire de l'albumine est trouvée sur la membrane des hépatocytes du foie et du chimpanzé humains que dans l'essence et est déterminée par le tropisme de HBV au foie humain et au chimpanzé.
Avec la pénétration du virus dans les hépatocytes sont libérés de l'ADN viral qui entre dans le noyau des hépatocytes et agissant en tant que matrice pour la synthèse d'acides nucléiques, lance une série de réactions biologiques successives, dont le résultat devient ensemble de nucléocapside du virus. Nucleocapsid migre à travers la membrane nucléaire dans le cytoplasme, où l'assemblage final des particules de Dane - le virus de l'hépatite B totale - a lieu.
Il convient de noter, cependant, que lorsqu'un hépatocyte est infecté, le processus peut aller de deux façons - réplicative et intégrative. Dans le premier cas, une image d'hépatite aiguë ou chronique se développe, et dans le second cas, un virus porteur.
Les causes qui prédéterminent les deux types d'interaction de l'ADN viral et de l'hépatocyte ne sont pas exactement établies. Très probablement, le type de réponse est génétiquement déterminé.
Le résultat d'interactions deviennent des structures d'assemblage réplicatives korovskogo antigène (dans le noyau) et l'assemblage complet du virus (dans le cytoplasme), suivie de la présentation d'un virus complet ou ses antigènes sur la membrane ou dans la structure de la membrane des hépatocytes.
On pense que la réplication du virus n'entraîne pas de dommage cellulaire au niveau des hépatocytes, puisque le virus de l'hépatite B n'a pas d'effet cytopathogène. Cette situation ne peut pas être considérée comme certaine, car elle est fondée sur des données expérimentales qui, bien qu'il n'y ait aucune preuve de l'effet cytopathique du virus de l'hépatite B, mais produit en culture tissulaire, et ne peut donc pas être entièrement extrapolés à l'hépatite virale B chez l'homme. Dans tous les cas, la question de l'absence de lésion des hépatocytes au cours de la phase réplicative nécessite une étude complémentaire.
Cependant, quelle que soit la nature de l'interaction du virus avec la cellule, le foie ci-après nécessairement inclus dans le processus immunopathologique. Ainsi, les dommages des hépatocytes en raison du fait que l'expression des antigènes viraux sur la membrane des hépatocytes et la libération d'antigènes viraux dans le circuit de circulation libre est commuté sur les réponses immunitaires cellulaires et humorales dirigées consécutives finalement l'élimination de l'organisme de virus yle. Ce processus est réalisé en pleine conformité avec les lois générales de la réponse immunitaire aux infections virales. Pour l'élimination de l'agent pathogène comprennent des réponses cellulaires cytotoxiques à médiation par des classes différentes de cellules effectrices: cellules K, les lymphocytes T, les cellules tueuses naturelles, les macrophages. Au cours de ces réactions est la destruction des hépatocytes infectés, qui est accompagnée par la libération d'antigènes viraux (HBcAg, NVeAg, HBsAg), le déclenchement d'un système d'anticorps, moyennant quoi des anticorps spécifiques accumulent dans le sang, en particulier à la vache - anti-HBc et l'antigène e - anti-HBE . Par conséquent, la libération de cellules hépatiques par le virus se produit au cours de sa mort en raison des réactions de cytolyse cellulaire.
Simultanément, des anticorps spécifiques s'accumulant dans le sang lient les antigènes du virus, formant des complexes immuns phagocytés par les macrophages et sécrétés par les reins. Ainsi, il peut y avoir différentes lésions immun glomérulonéphrite, artérite, arthralgies, éruptions cutanées, et d'autres. Depuis la participation d'anticorps spécifiques est l'organisme purifié de l'agent pathogène et il y a une récupération complète.
Conformément au concept précédent pathogenèse de l'hépatite B toutes les variantes cliniques multiples de maladie prises pour expliquer les caractéristiques de l'interaction des sous-traitants de virus et de cellules immunitaires, en d'autres termes, la puissance de la réponse immunitaire de la présence d'antigènes viraux. Selon les idées modernes, la force de la réponse immunitaire est génétiquement déterminée et liée aux antigènes d'histocompatibilité du locus HLA de première classe.
On pense généralement que dans les conditions d'une réponse immunitaire adéquate aux antigènes du virus, une hépatite aiguë avec une évolution cyclique et une récupération complète est cliniquement développée. Avec la réduction de la réponse immunitaire aux antigènes exprimés par cytolyse immunitaire à médiation virale légèrement, donc il n'y a pas d'élimination efficace des cellules du foie infectées, ce qui conduit à des manifestations cliniques fades avec la persistance prolongée du virus et peuvent développer une hépatite chronique. Dans ce cas, au contraire, dans le cas d'génétiquement déterminé une forte réponse immunitaire et la massivité de l'infection (transfusion sanguine) provoquent la zone étendue de la destruction des cellules hépatiques, qui correspondent à la forme clinique grave et maligne de la maladie.
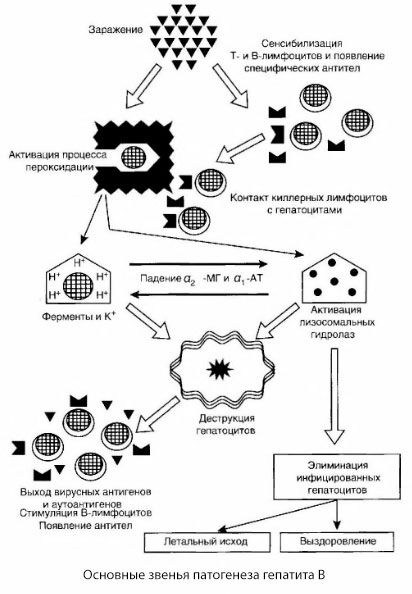
Le schéma présenté de la pathogenèse de l'hépatite B est remarquable pour son harmonie, néanmoins, il y a un certain nombre de moments contestables et peu-recherchés en elle.
Si nous suivons le concept de l'hépatite B comme une maladie immunopathologique, nous pourrions nous attendre à une augmentation des réactions de cytotoxicité cellulaire avec une augmentation de la gravité de la maladie. Cependant, dans les formes sévères, les indices du lien cellulaire de l'immunité sont fortement réduits, y compris une goutte multiple, en comparaison avec ceux chez les enfants en bonne santé, et un indice de cytotoxicité des cellules K. Quand une forme maligne lors du développement d'une nécrose hépatique massive et le coma hépatique particulièrement marqué incapacité totale à faire sauter la transformation des lymphocytes sous la fitogemattlyutinina influence, endotoxine Staphylococcus et HBsAg. En outre, il n'y a pas de capacité de leucocytes à migrer selon l'inhibition de la migration leucocytaire de réaction (RTML), et a révélé une augmentation dramatique des lymphocytes de perméabilité de la membrane à partir de ces études avec une tetracycline de la sonde fluorescente.
Ainsi, si les indicateurs de fluorescence de lymphocytes humains en bonne santé sont 9,9 ± 2%, et l'hépatite B typique avec bénigne, ils augmentent à 22,3 ± 2,7%, le nombre de formes malignes lymphocytes atteint en fluorescentes moyenne 63,5 ± 5,8%. Depuis l'augmentation de la perméabilité des membranes cellulaires sans ambiguïté évaluée dans la littérature comme un indicateur fiable de l'incapacité fonctionnelle, on peut conclure que l'hépatite B, notamment sous forme maligne, les dommages se produit brut des lymphocytes. Ceci est également mis en évidence par les indices de l'activité cytotoxique des cellules K. Dans une grave maladie cytotoxicité 1-2 semaines est de 8,8% ± 15,5, alors que pour une forme maligne de la 1ère semaine - 6,0 ± 2,6, le 2 - 22,0 ± 6,3% à la norme est de 44,8 ± 2,6%.
Les données présentées montrent clairement les perturbations prononcées dans l'immunité cellulaire chez les patients atteints de l'hépatite B. Sévère Il est également clair que ces changements se produisent une seconde fois, entraînant la défaite des cellules immunocompétentes par des métabolites toxiques et éventuellement en circulation complexes immuns.
Des études ont montré que chez les patients atteints d'hépatite sévère, en particulier dans le cas d'une nécrose du foie massif, du sérum sanguin est un titre tombant HVsAg et NVeAg et de commencer simultanément à détecter dans des titres élevés d'anticorps dirigés contre l'antigène de surface, ce qui est tout à fait inhabituel pour une forme bénigne de la maladie, lorsque quels anti-HBV n'apparaissent que le 3-5ème mois de la maladie.
La disparition rapide des antigènes du virus de l'hépatite B avec la présence simultanée de titres élevés d'anticorps antiviraux permet d'envisager la formation intensive de complexes immuns et leur participation possible à la pathogenèse du développement de la nécrose hépatique massive.
Ainsi, les matériaux réels ne permettent pas une interprétation sans équivoque de l'hépatite B seulement du point de vue de l'agression immunopathologique. Et ce n'est pas seulement le fait que ce ne se trouve pas la relation entre la profondeur et l'étendue des changements morphologiques dans le foie, d'une part, et le degré de facteurs d'immunité cellulaire - de l'autre. En théorie, ce fait pourrait expliquer les études de date ultérieure de l'immunité cellulaire, les cellules immunitaires lorsqu'il est soumis à un puissant effets toxiques dus à l'augmentation de l'insuffisance hépatique fonctionnelle. Vous pouvez, bien sûr, on suppose que la cytolyse immunitaire des hépatocytes se produit dans les stades de l'infection plus tôt, peut-être même avant l'apparition des symptômes cliniques de la maladie grave du foie. Cependant, une telle hypothèse est peu probable puisque chez les patients atteints aiguë (foudre) de la maladie a révélé des indices similaires de l'immunité cellulaire et, en plus, l'étude morphologique du tissu hépatique n'a pas été trouvé infiltration lymphocytaire massives en même temps détecté champ continu épithélium nécrotique sans signes de résorption et lymphocytaire agression.
Expliquer l'image morphologique dans l'hépatite aiguë seulement du point de vue de la cytolyse cellulaire immunitaire est très difficile, donc dans les premiers travaux n'excluait pas l'effet cytotoxique du virus de l'hépatite B.
À l'heure actuelle, cette hypothèse a été partiellement confirmée par la découverte du virus de l'hépatite B Des études ont montré que la fréquence de détection des marqueurs de l'hépatite D est directement proportionnelle à la gravité de la maladie: la forme bénigne, ils se trouvent dans 14%, modérée - 18 ans, sévère - 30 maligne - chez 52% des patients. Étant donné que le virus de l'hépatite D a nekrozogennym effet cytopathologique, il a été établi que dans le développement des formes fulminantes de l'hépatite B co-infection de grands virus de l'hépatite B et D. Importance
La pathogenèse de l'hépatite B peut être représentée comme suit. Après pénétration du virus de l'hépatite B dans les hépatocytes, une attaque immunologique est induite sur les hépatocytes infectés par les T-tueurs, qui libèrent les lymphotoxines vers les cellules hépatiques.
Les mécanismes intimes de la destruction des hépatocytes dans l'hépatite B n'ont pas été établis à ce jour. Le rôle principal est joué par des processus activés de peroxydation des lipides et des hydrolases lysosomales. Le point de départ peut être les lymphotoxines libérées par les cellules effectrices lorsqu'elles entrent en contact avec les hépatocytes, mais il est possible que le virus lui-même soit l'initiateur des processus de réoxydation. À l'avenir, le processus pathologique se développe probablement dans la séquence suivante.
- Interaction des facteurs d'agression (lymphotoxines ou virus) avec des macromolécules biologiques (éventuellement avec des composants de la membrane du réticulum endoplasmique, capables de prendre part à un processus de désintoxication, par analogie avec d'autres agents nuisibles, comme on l'a représenté en relation avec le tétrachlorure de carbone).
- Formation de radicaux libres, activation des processus de peroxydation lipidique et augmentation de la perméabilité de toutes les membranes hépatocellulaires (syndrome de cytolyse).
- Le mouvement des substances biologiquement actives le long du gradient de concentration est la perte d'enzymes de diverses localisations intracellulaires, de donneurs d'énergie, de potassium, etc. L'accumulation de sodium, de calcium et de pH se déplace vers l'acidose intracellulaire.
- Activation et rendement des hydrolases lysosomales (ARN-ase, ADN-ase, cathepsines, etc.) avec la désintégration de la cellule hépatique et la libération d'autoantigènes.
- Stimulation des systèmes T et B de l'immunité avec la formation d'une sensibilisation spécifique des lymphocytes T à la lipoprotéine hépatique, ainsi que la formation d'auto-anticorps humoraux anti-hépatiques.
Dans la pathogenèse du schéma proposé de l'hépatite B en tant que facteur de déclenchement sont les antigènes viraux dont les produits à forte intensité observée dans les premiers stades de la maladie et la période aiguë, sauf formes malignes dans lesquelles la production d'antigènes viraux est arrête presque au moment de la nécrose hépatique massive, qui prédétermine réduction rapide de la réplication virale.
Il est également évident que les antigènes viraux activent les systèmes T et B de l'immunité. Au cours de ce processus, une redistribution caractéristique des sous-populations de lymphocytes T survient, visant à organiser une réponse immunitaire adéquate, éliminant les hépatocytes infectés, neutralisant les antigènes viraux, la sanogenèse et la récupération.
Dans la réaction des cellules immunitaires à des antigènes viraux sur des hépatocytes ou des membranes lors de la réplication virale dans les hépatocytes, il existe des conditions pour l'activation de la peroxydation des lipides, la commande comme cela est connu, la perméabilité des membranes cellulaires et sous-cellulaires,
De ce point de vue, il devient compréhensible qu'un tel phénomène naturel et hautement caractéristique de l'émergence de l'hépatite virale du syndrome de cytolyse - augmentation de la perméabilité des membranes cellulaires
Le résultat final du syndrome de cytolyse peut être une dissociation complète de la phosphorylation oxydative, la sortie du matériel cellulaire, la mort du parenchyme hépatique.
Cependant, dans la très grande majorité des cas, ces processus n'atteignent pas un tel développement fatal. Seulement dans les formes malignes du processus pathologique de la maladie se produit comme une avalanche, et de manière irréversible, parce qu'il ya infestation massive, marquée processus immunitaire, l'activation excessive des processus et suroxydation lysosomales phénomènes gidrodaz agression auto-immune.
Ces mêmes mécanismes observés avec une évolution favorable de l'hépatite B, la seule caractéristique qu'ils sont mis en œuvre à un niveau qualitativement différent. Contrairement aux cas de nécrose hépatique massive, avec une évolution clinique favorable des hépatocytes infectés, et la zone où immunopathologique cytolyse peroxydation moins lipidique amplifié n'est pas si importante, l'activation des hydrolases acide conduit seulement à une autolyse limitée avec une libération négligeable de autoantigènes, et par conséquent, sans auto-agression massive soit toutes les étapes de la pathogenèse avec un cours favorable réalisées dans le cadre de l'organisation structurelle en cours de pas foie renhimy et des systèmes de protection (anti-oxydants, contraintes inhibiteurs, etc.) et ne dispose donc pas une telle action destructrice.
Les causes des symptômes d'intoxication dans l'hépatite virale ne sont pas complètement étudiées. La proposition de distinguer entre l'intoxication dite primaire, ou virale, et secondaire (métabolique ou métabolique) peut être considérée comme positive, bien que cela ne révèle pas le mécanisme intime de l'apparition du syndrome toxique général. Premièrement, les virus de l'hépatite n'ont pas de propriétés toxiques et, deuxièmement, la concentration de nombreux métabolites ne correspond pas toujours à la gravité de la maladie et au degré de symptômes de toxicose. On sait également que la concentration des antigènes viraux n'est pas strictement corrélée avec la gravité de l'intoxication. Au contraire, avec une augmentation de la sévérité de la maladie et, par conséquent, une augmentation du degré de toxicose, la concentration de HBsAg diminue et est la plus faible dans les formes malignes au moment de l'apparition du coma hépatique profond. Cependant, la fréquence de détection et les titres d'anticorps antiviraux spécifiques dépendent directement de la gravité de la maladie.
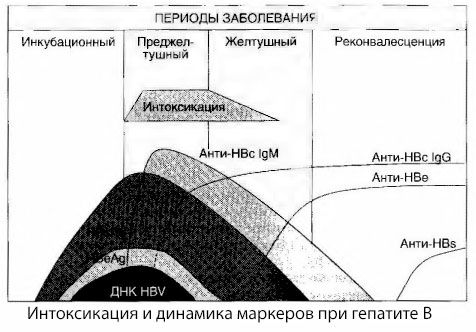
Intoxication ne semble pas au moment de l'enregistrement des antigènes viraux, et la période de circulation des anticorps IgM antiviral sanguin à l'antigène et le système antigène korovskomu E. En outre, lorsque les formes lourdes et surtout malignes une partie importante du sang des patients apparaissent même anti-HBs, qui généralement jamais observé avec des formes légères et modérées de la maladie.
Les données présentées permet de conclure que le toxicosis syndrome de l'hépatite virale et l'hépatite B en particulier, ne se pose pas en raison d'antigènes viraux dans le sang et est une conséquence de l'interaction des antigènes viraux avec des anticorps IgM anti-viraux. Le résultat d'une telle interaction, comme on le sait, est la formation de complexes immuns et, éventuellement, de substances toxiques actives.
Les symptômes d'intoxication surviennent au moment de l'apparition de complexes immuns en circulation libre, mais à l'avenir, une telle corrélation ne peut être tracée.
Une explication partielle à cela peut être trouvée dans l'étude de la composition des complexes immuns. Chez les patients atteints Circulate sanguine sévère systèmes principalement de taille moyenne, et dans leur composition à une altitude de syndrome toxique dominé par les anticorps de classe alors que dans la récession, et les manifestations cliniques des systèmes de récupération deviennent plus grandes, et ils commencent à dominer la composition d'anticorps IgG.
Les données présentées concernent les mécanismes du développement du syndrome toxique dans la période initiale de la maladie, mais avec une toxicose survenant au plus fort des manifestations cliniques, elles n'ont qu'une importance partielle et surtout dans le développement du coma hépatique.
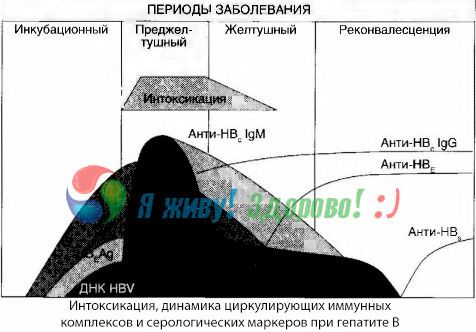
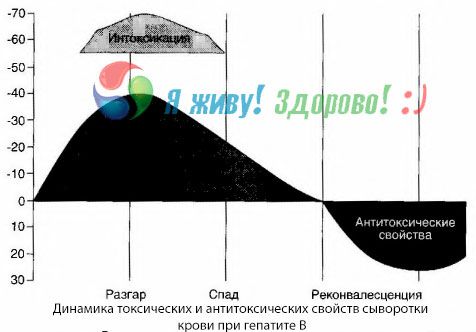
Par la méthode des hémocultures, il a été possible de montrer que dans l'hépatite B, le sang accumule constamment des toxines libérées du tissu hépatique en décomposition affecté. La concentration de ces toxines est proportionnelle à la gravité de la maladie, elles sont de nature protéique.
Pendant la période de convalescence, des anticorps dirigés contre cette toxine apparaissent dans le sang; mais dans le cas d'un coma hépatique, la concentration de la toxine dans le sang augmente brusquement et les anticorps dans le sang ne sont pas détectés.
Pathomorphologie de l'hépatite B
Par la nature des changements morphologiques, il existe trois formes d'hépatite B aiguë:
- forme cyclique,
- nécrose massive du foie;
- hépatite péricholangiolytique cholestatique.
Lorsque la forme cyclique des modifications dégénératives de l'hépatite B, inflammatoires et prolifératives étaient plus prononcés dans les lobules du centre, tandis que l'hépatite A, ils sont situés à la périphérie des tranches, la propagation vers le centre. Ces différences s'expliquent par différentes voies de pénétration du virus dans le parenchyme du foie. L'hépatite A virus pénètre dans le foie par la veine porte et se prolonge vers le centre des lobules, le virus de l'hépatite B pénètre par l'artère hépatique et les capillaires de ramification d'alimentation de manière uniforme tous les segments, jusqu'à leur centre.
Le degré de défaite du parenchyme hépatique correspond dans la plupart des cas à la sévérité des manifestations cliniques de la maladie. Dans des formes plus douces observé habituellement une nécrose focale des hépatocytes, et à des formes modérées et sévères - nécrose zonale (avec une tendance à la formation de ponts de fusion et la nécrose dans les formes sévères de la maladie).
Les plus grands changements morphologiques dans le parenchyme sont observés à la hauteur des manifestations cliniques, qui coïncident habituellement avec la 1 ère décennie de la maladie. Au cours de la deuxième et surtout de la troisième décennie, les processus de régénération sont intensifiés. A ce moment, les changements nécrobiotiques disparaissent presque complètement et les processus d'infiltration cellulaire avec une lente restauration ultérieure de la structure des plaques cellulaires hépatiques commencent à prédominer. Cependant, la restauration complète de la structure et de la fonction du parenchyme hépatique survient seulement 3 à 6 mois après le début de la maladie et pas tous les patients.
Infection généralisée par l'hépatite B et confirmé par la détection de HBsAg, non seulement dans les hépatocytes, mais aussi dans les reins, les poumons, la rate, le pancréas, les cellules de la moelle osseuse, et d'autres.
Cholestatique (periholangiolitichesky) hépatite - une forme particulière de la maladie, dans lequel les plus grands changements morphologiques sont détectés par les conduits biliaires intra-hépatiques, et avec une image holangiolita periholangiolita. Dans cholestase forme cholestatique se produire une expansion du capillaire de bile avec une stase biliaire dans les cholangioles prolifération et l'infiltration cellulaire qui les entoure. Les cellules hépatiques avec cette forme d'hépatite sont légèrement affectées. Cliniquement, la maladie est caractérisée par une évolution prolongée avec un ictère prolongé. Il est démontré que la raison de ce genre de maladie servent d'effet préventif du virus sur le mur à cholangioles effet négligeable sur les hépatocytes.

