Expert médical de l'article
Nouvelles publications
Ostéoblastoclastome
Dernière revue: 04.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
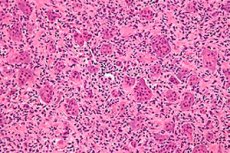
Les cas de maladies oncologiques sont en constante augmentation dans le monde. Parmi les lésions du système squelettique, l'ostéoblastoclastome (tumeur à cellules géantes, ostéoclastome) est la plus fréquente. Il s'agit d'une tumeur bénigne à tendance maligne, capable d'endommager divers os du squelette. [ 1 ] Le tableau clinique initial de la maladie passe inaperçu, mais avec le temps, un gonflement d'une zone osseuse spécifique attire l'attention: la tumeur grossit progressivement et sans douleur. Le traitement de cette pathologie est chirurgical, impliquant l'ablation de l'ostéoblastoclastome au niveau des tissus sains. Avec un traitement rapide, l'évolution de la maladie est jugée encourageante. [ 2 ]
Épidémiologie
La première description détaillée de cette tumeur a été donnée par le chirurgien français Auguste Nélaton au XIXe siècle. Cette formation de cellules géantes était classée dans la catégorie des ostéodystrophies fibreuses. Cette pathologie a été désignée par différents termes: tumeur brune, gigantome, ostéoclastome, ostéodystrophie fibreuse locale, sarcome à cellules géantes. Le nom d'ostéoblastoclastome a été introduit dans la terminologie médicale par le professeur Rusakov.
Aujourd'hui, les spécialistes n'ont aucun doute sur l'origine tumorale de l'ostéoblastoclastome, considéré comme l'une des tumeurs osseuses les plus fréquentes. La maladie touche à peu près aussi bien les hommes que les femmes. Il existe des descriptions de pathologies familiales et héréditaires.
L'ostéoblastoclastome peut se développer à presque tout âge. Des cas de tumeurs ont été détectés chez des nourrissons d'un an et des personnes âgées de 70 ans. Selon les statistiques, près de 60 % des patients atteints de ce type de néoplasme ont entre 20 et 30 ans.
L'ostéoblastoclastome appartient à la catégorie des tumeurs solitaires, généralement isolées. De tels foyers se développent rarement dans les tissus osseux adjacents. La lésion s'étend le plus souvent aux os tubulaires longs (près de 75 % des cas), les os petits et plats étant un peu moins souvent touchés.
Les os tubulaires longs sont principalement touchés au niveau de l'épimétaphyse (chez l'enfant, au niveau de la métaphyse). On n'observe pas de croissance tumorale dans les tissus du cartilage articulaire et épiphysaire. Plus rarement, la pathologie touche la diaphyse (moins de 1 % des cas).
L'ostéoblastoclastome des os du visage représente plus de 20 % de toutes les tumeurs trouvées à cet endroit.
Les spécialistes distinguent les ostéoblastoclastomes malins des ostéoblastoclastomes bénins. Les pathologies malignes sont rares chez l'enfant.
Causes ostéoclastomes
Les médecins ne parviennent pas à identifier une cause précise du développement de l'ostéoblastoclastome. On pense que l'apparence de la pathologie peut être influencée par:
- processus inflammatoires affectant l'os et le périoste;
- blessure traumatique ou blessures répétées sur la même zone osseuse;
- irradiations répétées;
- perturbation de la formation osseuse pendant la période prénatale.
Dans environ sept cas sur dix, l’ostéoblastoclastome affecte les os tubulaires longs, mais il peut se propager aux tendons et aux tissus mous voisins.
Si la pathologie se développe dans la région maxillo-faciale, la cause est le plus souvent une lésion osseuse ou un processus infectieux, par exemple après une extraction dentaire. Plus rarement, on observe une néoplasie au niveau du péroné et du tibia, des côtes et de la colonne vertébrale.
Les femmes souffrent souvent d'une tumeur ténosynoviale à cellules géantes diffuse au niveau des mains, des orteils, des fémurs et des genoux. Cette tumeur se présente sous la forme d'une formation dense au sein des tissus mous, localisée près des tendons. Progressivement, le processus s'étend à l'os articulaire, le lésant et le détruisant.
En général, les causes de l’ostéoblastoclastome sont considérées comme étant les suivantes:
- changements dans l'équilibre hormonal;
- pathologies endocriniennes;
- exposition aux risques professionnels, mauvaises habitudes;
- mauvaise nutrition;
- utilisation à long terme ou incorrecte de certains médicaments;
- lésions parasitaires;
- séjour prolongé en zone radioactive.
La transformation d'un ostéoblastoclastome bénin en tumeur maligne est possible sous l'influence de:
- blessures fréquentes du segment osseux pathologiquement altéré;
- changements hormonaux importants (par exemple, pendant la grossesse);
- irradiation répétée.
Les facteurs énumérés ci-dessus ne conduisent pas nécessairement au développement d’une pathologie, mais ils peuvent avoir un impact négatif sur les personnes prédisposées au développement d’un ostéoblastoclastome.
Facteurs de risque
L'ostéoblastoclastome se développe le plus souvent chez les patients de plus de 10 ans. Chez les enfants de moins de 5 ans, cette pathologie est très rare.
Le risque de développer une tumeur augmente sous l’influence des facteurs suivants:
- Conditions environnementales défavorables, présence de risques professionnels et domestiques, intoxications, maladies infectieuses chroniques, infestations parasitaires.
- Antécédents de pathologies oncologiques, radiothérapie antérieure (notamment plusieurs cures), autre exposition aux rayonnements (y compris le fait de vivre ou de travailler dans des régions radioactivement dangereuses).
- Blessures fréquentes, fractures, contusions, fissures osseuses.
- Facteurs génétiques, changements ou mutations génétiques, diagnostics de cancer chez des proches parents.
- Anomalies osseuses congénitales, troubles de la structure squelettique.
Souvent, le facteur environnemental n'est pas considéré comme la cause principale, et ce à tort: les problèmes environnementaux ont un impact direct sur la qualité de l'air, des produits alimentaires et du régime hydrologique local, ce qui affecte invariablement la santé. Les effets néfastes des rayons ultraviolets sont observés chez les personnes fréquentant les plages et les piscines ouvertes pendant une longue période et attrapent régulièrement des coups de soleil.
L’influence des substances cancérigènes et des radiations se retrouve également dans de nombreuses industries dangereuses impliquant des produits chimiques tels que le nickel, l’amiante, l’acide sulfurique, l’arsenic, ainsi que le traitement des métaux et du plastique.
Pathogénèse
La tumeur à cellules géantes est une lésion osseuse complexe, histologiquement bénigne, qui récidive rarement, bien qu'elle soit certainement source de métastases bénignes et se transforme fréquemment en sarcome après irradiation. En l'absence d'origine histogénétique claire, la tumeur à cellules géantes doit son nom à son aspect histologique spécifique.
La description morphologique typique est celle d'une lésion bénigne des cellules stromales mononucléaires, avec une abondance de cellules géantes bénignes de type ostéoclaste. Les études immunohistochimiques et moléculaires des tissus d'ostéoclastome mettent en évidence deux populations de cellules stromales: l'une composée de cellules fusiformes prolifératives, marqueurs d'origine ostéoblastique[ 3 ],[ 4 ], tandis que l'autre population est constituée de cellules polygonales marquées par les antigènes monocytes/macrophages CD14+/CD68+[ 5 ].
Les principales caractéristiques pathogéniques de l'ostéoblastoclastome:
- La tumeur comprend deux types de cellules: les cellules géantes multinucléées et les petites cellules mononucléées;
- le segment distal du fémur, le segment proximal du tibia, le segment distal du radius, ainsi que les os du bassin et l'omoplate (moins souvent la colonne vertébrale) sont les plus souvent touchés;
- la lésion est majoritairement isolée et solitaire;
- la tumeur est située dans l'épiphyse ou la métaphyse, qui gonfle considérablement, se déforme sous la forme d'un gros tubercule ou d'un hémisphère;
- le processus pathologique atteint le cartilage articulaire et est interrompu;
- le néoplasme se développe dans toutes les directions, mais la croissance principale est observée le long de l'axe de l'os long vers la diaphyse;
- la dimension transversale augmente diamétralement de plus de trois fois;
- dans la variante cellulaire de l'ostéoblastoclastome, le néoplasme est constitué de chambres séparées les unes des autres par des barrières complètes et partielles (comme de la mousse de savon ou des nids d'abeilles irréguliers);
- il y a une divergence du cortex, un gonflement de l'intérieur, un amincissement, sans couches périostées;
- si l'ostéoblastoclastome est de taille importante, alors le cortex est résorbé, le néoplasme est entouré d'une fine capsule coquillière constituée des parois des chambres superficielles;
- dans la variante ostéolytique, il n'y a pas de motif de chambre, le défaut osseux est homogène;
- défaut marginal en forme de soucoupe;
- on observe une résorption de la couche corticale, la croûte devient plus nette au niveau de la ligne de lésion, sans saper ni les couches périostées;
- le défaut a des contours nets;
- des fractures pathologiques sont observées chez 12 % des patients.
L'ostéoblastoclastome affecte les zones riches en moelle osseuse myéloïde. On observe souvent des courbures et un raccourcissement osseux prononcés, notamment en cas de retard de diagnostic et de traitement. Dans la plupart des cas, la tumeur est excentrique, avec destruction de la grande majorité des condyles osseux. Radiologiquement, on observe une atteinte de la couche osseuse sous-chondrale. Dans près de la moitié des cas, l'extrémité articulaire de l'os est entièrement touchée, qui gonfle, la couche corticale est détruite et la lésion s'étend au-delà des limites osseuses.
Aujourd’hui, l’ostéoblastoclastome est rarement considéré comme une tumeur bénigne: il est classé comme un néoplasme agressif, principalement en raison de son imprévisibilité et de sa forte probabilité de malignité.
Symptômes ostéoclastomes
Les manifestations cliniques sont quasiment identiques chez l'enfant et la personne âgée. Les premiers signes ne sont pas immédiatement détectés, car l'ostéoblastoclastome se développe initialement de manière latente et ne peut être identifié que près d'un an après son apparition.
Les experts distinguent les symptômes généraux des symptômes locaux. Les signes généraux accompagnent généralement l'ostéoblastoclastome malin, tandis que les signes locaux sont présents dans les néoplasies bénignes.
Les symptômes généraux ne dépendent pas de la localisation de l’os affecté:
- douleur intense dans la zone de croissance tumorale;
- palpation craquement, indiquant la croissance du néoplasme et la destruction du segment osseux;
- l’apparition d’un réseau de vaisseaux au-dessus du foyer pathologique;
- une augmentation constante des ballonnements;
- douleur croissante à mesure que la tumeur grandit;
- altération de la fonction musculaire et articulaire à proximité de la zone affectée;
- hypertrophie des ganglions lymphatiques voisins;
- malaise général, fatigue;
- augmentation de la température corporelle;
- perte d’appétit, perte de poids;
- apathie, impuissance.
Les manifestations locales sont liées à la localisation de l'os affecté. Par exemple, si un ostéoblastoclastome se développe dans l'une des mâchoires, la symétrie faciale est progressivement perturbée. Le patient commence à éprouver des difficultés d'élocution et de mastication, et parfois, les dents se déchaussent et tombent. Dans les cas graves, des zones nécrotiques et des fistules se forment.
90 % des tumeurs à cellules géantes présentent une localisation épiphysaire typique. La tumeur s'étend souvent à l'os sous-chondral articulaire, voire touche le cartilage. L'articulation et/ou sa capsule sont rarement atteintes. Dans les rares cas d'ostéoclastome chez l'enfant, la lésion est le plus souvent métaphysaire. [ 6 ], [ 7 ] Les sites les plus fréquents sont, par ordre décroissant, le fémur distal, le tibia proximal, le radius distal et le sacrum. [ 8 ] 50 % des ostéoclastomes surviennent dans la région du genou. Les autres sites fréquents incluent la tête du péroné, le fémur proximal et l'humérus proximal. La localisation pelvienne est rare. [ 9 ], [ 10 ] La multicentricité, ou l'apparition simultanée d'ostéoclastomes dans différents sites squelettiques, est connue, mais extrêmement rare. [ 11 ], [ 12 ]
Si un ostéoblastoclastome se développe dans les jambes, la démarche du patient se modifie. Avec le temps, les muscles du membre inférieur endommagé s'atrophient et la marche devient difficile. Dans certains cas, des processus osseux dystrophiques apparaissent, l'os s'amincissant. Des fractures pathologiques surviennent, accompagnées de douleurs intenses et d'un gonflement des tissus. Des complications telles qu'hémorragies, hématomes et nécrose des tissus mous peuvent survenir.
Si l'ostéoblastoclastome se développe dans la région de l'humérus ou du fémur, la motricité des phalanges des doigts et la fonction globale du membre affecté sont altérées.
Lorsque la tumeur devient maligne, l'état du patient s'aggrave. Les signes suivants sont à noter:
- la douleur dans la zone affectée de l'os augmente;
- le néoplasme se développe régulièrement;
- le tissu osseux est détruit, la zone de cette destruction s'étend;
- le foyer tumoral perd ses limites nettes;
- la couche corticale est détruite.
Seul un spécialiste peut constater de tels changements lors d’un diagnostic instrumental.
Les ostéoblastoclastomes bénins se caractérisent par une évolution progressive, latente ou asymptomatique. Le syndrome douloureux n'apparaît que pendant la progression de la pathologie; après plusieurs mois, le patient commence à ressentir une douleur irradiante. Chez de nombreux patients, le premier signe de la maladie est une fracture pathologique. Au moment du diagnostic, environ 12 % des patients atteints d'ostéoclastome présentent une fracture pathologique. [ 13 ], [ 14 ] On pense que la présence d'une fracture pathologique indique une maladie plus agressive, avec un risque accru de récidive locale et de métastase. [ 15 ]
Lorsque l'ostéoblastoclastome devient malin, la tumeur, jusque-là à peine visible, devient douloureuse et des signes d'irritation des terminaisons nerveuses sont détectés. Si la tumeur est principalement maligne, la douleur est intense et invalidante, avec une aggravation rapide du tableau neurologique.
Ostéoblastoclastome chez les enfants
Les signes cliniques des différentes formes d'ostéoblastoclastome bénin sont souvent différents. Les formes kystiques sont asymptomatiques pendant longtemps et, dans 50 % des cas, ne sont détectées qu'après le développement d'une fracture pathologique. Le processus tumoral est détecté par une prolifération tissulaire intraosseuse importante, accompagnée d'un syndrome douloureux. La protrusion d'une section osseuse n'apparaît qu'en cas de prolifération prononcée: le patient présente un réseau veineux élargi et une mobilité articulaire limitée. La forme lytique de l'ostéoblastoclastome se caractérise par une croissance plus rapide et une apparition précoce de la douleur, mais les contractures sont moins fréquentes.
Le plus souvent, chez l'enfant, l'ostéoblastoclastome affecte les métaphyses supérieures de l'humérus et du fémur. Plus rarement, des lésions sont observées au niveau de la métaphyse fémorale inférieure, du tibia et du péroné. Dans la forme lytique, une destruction du cartilage épiphysaire est possible, avec une extension à l'épiphyse, sans pénétration dans l'articulation (le cartilage articulaire reste intact). Dans la forme kystique active, une croissance tumorale est observée dans la partie centrale de la diaphyse, avec un amincissement marqué de la couche corticale et un gonflement osseux.
Les ostéoblastoclastomes infantiles sont généralement bénins, mais ils peuvent également provoquer une destruction osseuse importante. La croissance du cartilage épiphysaire ralentit la croissance du membre, ce qui peut entraîner des fractures pathologiques, une pseudarthrose avec un défaut osseux prononcé et un syndrome douloureux.
Lors d'un processus malin, une tumeur de type sarcome ostéogène se forme: une croissance rapide et une destruction osseuse prononcée sont caractéristiques. Pour le diagnostic différentiel, les enfants subissent un examen histologique.
Étapes
Les experts distinguent les stades lytiques et cellulaires-trabéculaires du développement de l'ostéoblastoclastome.
- Le stade cellulaire-trabéculaire est caractérisé par la formation de foyers de destruction du tissu osseux séparés par des cloisons.
- Le stade lytique se caractérise par la formation d'un foyer destructeur continu, localisé de manière asymétrique par rapport à l'axe central de l'os. À mesure que le néoplasme se développe, il peut s'étendre à toute la section osseuse.
Un signe typique d'ostéoblastoclastome est la séparation du foyer destructeur de la partie saine de l'os. Le canal médullaire est séparé du néoplasme par une plaque de fermeture.
Formes
En fonction des informations cliniques et radiologiques et des caractéristiques morphologiques, on distingue les principaux types d'ostéoblastoclastomes suivants:
- Le type cellulaire se rencontre principalement chez les patients d'âge moyen et les personnes âgées. La tumeur se développe lentement, se manifestant finalement par une tuméfaction dense à surface nodulaire, sans possibilité de limitation par l'os sain. Localisée au niveau de la mâchoire, cette dernière prend une forme fusiforme. La position des dents reste inchangée. Le tissu recouvrant l'ostéoblastoclastome cellulaire présente un caractère anémique. À la radiographie, on distingue une ombre formée par un grand nombre de formations kystiques et cellulaires, séparées les unes des autres par des barrières. Il n'y a pas de réaction du périoste.
- La forme kystique de l'ostéoblastoclastome provoque initialement des sensations douloureuses. À la palpation de la tumeur, certaines zones sont malléables et un « crissement de parchemin » est observé. L'os au-dessus de la tumeur s'amincit et prend une forme lisse, convexe et en forme de dôme. À la radiographie, la lésion ressemble à un kyste odontogène ou à un améloblastome.
- La pathologie lytique est relativement rare, principalement chez les enfants et les adolescents. La tumeur se développe assez rapidement. L'amincissement de la couche corticale provoque des douleurs: d'abord gênantes au repos, puis à la palpation de la zone affectée. On observe une expansion du réseau vasculaire au-dessus du site tumoral. Lorsque le foyer pathologique est localisé au niveau de la mâchoire, les dents deviennent tordues et se déchaussent. Des fractures pathologiques sont possibles. Une zone d'éclaircissement non structurée est visible sur la radiographie.
Selon le degré de malignité, l'ostéoblastoclastome est divisé en bénin (sans atypisme cellulaire), malin primaire et malin (transformé à partir d'une tumeur bénigne).
Selon la localisation, on distingue les types de pathologies suivants:
- La forme périphérique de l'ostéoblastoclastome sur la mâchoire supérieure ne présente pas de caractéristiques morphologiques particulières et est localisée sur les gencives.
- La forme centrale est située à l'intérieur de la structure osseuse et, contrairement à la forme périphérique, présente des zones hémorragiques, responsables de la teinte brune de la tumeur. La tumeur est représentée par un conglomérat.
- L'ostéoblastome de la mâchoire inférieure se localise dans l'épaisseur du tissu osseux, au niveau des molaires et des prémolaires. La croissance de la tumeur s'étend sur plusieurs années (en moyenne 3 à 10 ans), accompagnée d'une altération de la fonction de l'articulation temporo-mandibulaire.
- L'ostéoblastoclastome de la mâchoire supérieure se manifeste par une protrusion de la zone maxillaire affectée, un déchaussement des dents et une asymétrie faciale. La tumeur se développe lentement et sans douleur.
- L'ostéoblastoclastome du fémur est la localisation la plus fréquente, avec atteinte de la zone de croissance osseuse: le grand trochanter, le col et la tête du fémur. Plus rarement, le petit trochanter est atteint (de manière isolée). Cette pathologie s'accompagne de douleurs, de déformations osseuses et de fractures pathologiques.
- L'ostéoblastoclastome de l'ilion se développe le plus souvent à sa base. Il est également possible d'affecter le cartilage en Y avec destruction de la branche horizontale de l'os pubien ou de la branche descendante de l'ischion. La pathologie est initialement asymptomatique, puis des douleurs apparaissent à l'effort et une boiterie.
Complications et conséquences
La conséquence la plus défavorable de l'ostéoblastoclastome bénin est sa malignité. Les tumeurs malignes à cellules géantes sont rares; une analyse des études a révélé une fréquence de 1,6 % de tumeurs malignes primaires et de 2,4 % de tumeurs malignes secondaires. Une croissance infiltrante est détectée, les ganglions lymphatiques les plus proches sont touchés et des métastases peuvent se propager. [ 16 ]
L'ostéoblastome malin à cellules géantes est capable de produire les types de métastases suivants:
- chaud (se développant rapidement, détruisant activement les tissus environnants);
- froid (sans développement spécifique, existant depuis longtemps dans un état inactif, mais ayant la capacité de se transformer en « chaud »);
- muet (existant dans un état anabiotique et détecté par hasard).
L'ostéoblastoclastome malin peut se présenter sous trois formes:
- Une tumeur maligne primaire conserve son type de structure de base, mais il existe une atypicité des éléments mononucléaires et la présence de mitose dans ceux-ci.
- Malignité d'une tumeur principalement bénigne avec développement d'un sarcome à cellules fusiformes ou ostéogénique.
- Malignité après un traitement antérieur, notamment après des interventions non radicales ou une radiothérapie irrationnelle. Dans ce cas, un sarcome polymorphe avec métastases pulmonaires se développe le plus souvent.
L'ostéoclastome malin est généralement considéré comme un sarcome de haut grade; [ 17 ] cependant, les données des études suggèrent que l'ostéoclastome malin se comporte comme un sarcome de bas ou de grade intermédiaire. [ 18 ] Des métastases surviennent chez 1 à 9 % des patients atteints d'ostéoblastoclastome, et certaines études antérieures ont corrélé l'incidence des métastases avec une croissance agressive et une récidive locale. [ 19 ], [ 20 ]
Après des interventions chirurgicales, les patients dont la capacité de travail est limitée ou perdue se voient attribuer le groupe d’invalidité approprié.
Diagnostics ostéoclastomes
Pour diagnostiquer l'ostéoblastoclastome, il est nécessaire d'utiliser les méthodes suivantes:
- interrogatoire du patient, examen attentif et palpation de la zone osseuse affectée, étude de l'anamnèse;
- diagnostics de laboratoire et instrumentaux, études morphologiques.
Lors de l'anamnèse, le médecin examine les premières manifestations de la tumeur, la présence et la nature de la douleur, les antécédents médicaux et les blessures, les traitements antérieurs et l'état général. Il est également important de clarifier l'état des systèmes urinaire, reproducteur et respiratoire, du foie, des reins et des ganglions lymphatiques, et de réaliser une échographie des organes internes.
Des analyses de sang et d'urine sont prescrites à tous les patients, afin de doser les protéines et leurs fractions, les acides sialiques, le phosphore et le calcium. Il est également nécessaire de déterminer l'activité enzymatique des phosphatases, de réaliser un test de diphénylémie, d'évaluer la protéine C-réactive, etc. Il est à noter que les paramètres biologiques des tumeurs osseuses sont généralement non spécifiques, mais peuvent contribuer au diagnostic différentiel. Par exemple, en cas d'ostéoblastoclastome malin, des modifications telles qu'une leucocytose, une accélération de la VS, une diminution des protéines sanguines et du fer non hémoglobinique, ainsi qu'une augmentation des acides sialiques et des phosphatases alcalines sont possibles. De l'oxyproline et de l'hexokinase sont présentes dans les urines. Les taux de phosphore et de calcium sériques augmentent.
Les examens conventionnels en cas de suspicion d'ostéoblastoclastome comprennent des radiographies générales et ciblées, ainsi que la tomographie. La radiographie permet une localisation, une ampleur et une nature plus précises de la maladie, et permet de déterminer son extension aux organes et tissus environnants. La tomodensitométrie permet d'examiner les lésions pathologiques profondes et de déterminer la taille de la lésion osseuse. Cependant, l'imagerie par résonance magnétique (IRM) est considérée comme plus informative: à partir des informations obtenues, les médecins peuvent assembler une image spatiale, y compris une image tridimensionnelle.
Lors de l'examen morphologique, le matériel obtenu lors de l'aspiration et de la trépanobiopsie, ou les zones osseuses prélevées avec l'ostéoblastoclastome, sont étudiés. Une biopsie par ponction est réalisée à l'aide d'aiguilles spéciales et la tumeur est ponctionnée sous observation radiographique.
Lors de l'examen radiographique des os tubulaires longs, on observe un foyer ostéolytique destructeur, localisé de manière excentrique dans la région épiphysaire. En dynamique, la pathologie diverge vers le cartilage articulaire, ainsi que vers la métaphyse osseuse, et peut occuper toute la section transversale (ce qui est typique de l'ostéoblastoclastome de la tête du péroné et du radius). La couche corticale est fortement amincie, gonflée, et une destruction partielle est souvent détectée. Dans un processus bénin, il n'y a pas de réaction périostée. La frontière entre le néoplasme et la substance spongieuse est floue et floue. Dans la très grande majorité des cas, la limite sclérotique est absente.
En cas de lésion de la moelle épinière, la tumeur est localisée dans le corps vertébral dans 80 % des cas. Le corps vertébral, avec sa voûte et ses apophyses, peut être touché; parfois, plusieurs vertèbres, les sections costales et l'articulation sacro-iliaque sont impliquées dans le processus pathologique. Les foyers destructeurs peuvent avoir une structure cellulaire ou lytique.
L'étude des images stratifiées par tomodensitométrie révèle une destruction de l'arc avec les processus transverses, invisible sur une radiographie classique. L'IRM permet d'examiner l'impact de la tumeur sur la moelle épinière. [ 21 ], [ 22 ]
L'ostéoblastoclastome malin primitif se définit radiologiquement comme un foyer lytique destructeur aux limites floues. Dans certains cas, la structure est grossièrement maillée. On observe un gonflement de la zone osseuse affectée, un amincissement important de la couche corticale, suivi de sa destruction. La plaque corticale est hétérogène de l'intérieur. Une réaction périostée est possible.
Lors de la transformation maligne d'un ostéoblastoclastome initialement bénin, une structure à larges mailles, à fines mailles ou lytique du foyer destructeur est révélée. La zone osseuse affectée est « enflée », la couche corticale est très fine, avec des contours irréguliers sur la face interne. Une destruction corticale est possible. La réaction périostée (pic de Codman faible) a le caractère d'une périostite bulbeuse.
Pour détecter d’éventuelles métastases, une échographie est prescrite pour aider à étudier l’état des organes internes.
L'étape finale du diagnostic des tumeurs osseuses est l'identification histologique et l'examen cytologique des frottis. Le matériel est prélevé par biopsie (ouverte ou ponction).
Diagnostic différentiel
Les ostéoblastoclastomes bénins doivent être différenciés de toutes les pathologies présentant des signes de kyste osseux ou de lyse tissulaire à la radiographie. Ces pathologies comprennent:
- dysplasie fibreuse;
- sarcome ostéogénique lytique;
- ostéodystrophie parathyroïdienne;
- foyer de tuberculose osseuse;
- kyste osseux anévrismal.
En cas de lésions osseuses étendues et évolutives, il faut suspecter un ostéoblastoclastome. Cette tumeur se caractérise par l'absence d'ostéoporose osseuse périphérique, un processus destructeur à partir de la métaphyse et une pénétration tardive de la pathologie dans l'épiphyse.
Il est possible de différencier l'ostéodystrophie parathyroïdienne de l'ostéoblastoclastome uniquement à l'aide de la radiographie et d'études biochimiques.
Des difficultés peuvent survenir lors du diagnostic de l'ostéoblastoclastome des os tubulaires longs, ainsi que lors de la différenciation de la maladie du sarcome ostéogénique ou des formations kystiques (osseuses ou anévrismales).
La localisation d'un kyste anévrismal est principalement diaphysaire ou métaphysaire. En cas de localisation excentrique, on observe un gonflement osseux local, une fine couche corticale: le néoplasme est étiré le long de l'os et peut contenir des particules calcaires. En cas de localisation centrale, la métaphyse ou la diaphyse gonfle symétriquement, ce qui n'est pas le cas dans l'ostéoblastoclastome.
Chez l'enfant, l'ostéoblastoclastome peut être confondu avec l'ostéodysplasie fibreuse monostotique. Dans ce cas, l'os est déformé, raccourci (parfois allongé), mais ne gonfle pas, comme dans l'ostéoblastoclastome. L'ostéodysplasie fibreuse affecte principalement la métaphyse et la diaphyse des os tubulaires. La couche corticale peut s'épaissir, et des zones sclérotiques se forment autour des zones de destruction. Le processus de développement est indolore et lent.
Si l'ostéoblastoclastome affecte la mâchoire inférieure, la pathologie doit être différenciée de l'odontome, du fibrome osseux, de l'adamantinome et du kyste dentigère.
Qui contacter?
Traitement ostéoclastomes
L'objectif du traitement est de minimiser la morbidité et d'optimiser la fonctionnalité de l'os affecté; traditionnellement, ce traitement était réalisé par curetage intralésionnel avec comblement de la cavité. De nouvelles techniques, comme la cimentation osseuse, sont encourageantes car elles facilitent la reconstruction et réduisent les récidives locales.[ 23 ]
La seule façon de se débarrasser complètement de l’ostéoblastoclastome est la chirurgie: la tumeur est retirée, ce qui empêche d’autres dommages à l’os.
Les petits ostéoblastoclastomes sont soigneusement grattés à l'aide d'une curette spéciale. Le défaut osseux résultant est remplacé par autotransplantation. En cas de tumeur volumineuse, une résection osseuse est réalisée, suivie d'une chirurgie plastique. [ 24 ], [ 25 ], [ 26 ]
En raison du taux élevé (25 à 50 %) de récidive locale après curetage et greffe osseuse, les chirurgiens ont été encouragés à améliorer leurs procédures chirurgicales en utilisant des adjuvants chimiques ou physiques tels que l'azote liquide, le ciment acrylique, le phénol, le peroxyde d'hydrogène, la chimiothérapie locale ou la radiothérapie.[ 27 ],[ 28 ] Il a été démontré que la thérapie adjuvante locale aide à contrôler le taux de récidive.[ 29 ]
Si, pour une raison quelconque, une intervention chirurgicale est contre-indiquée chez le patient, une radiothérapie lui est prescrite. Grâce à la radiothérapie, il est possible d'arrêter la croissance de la tumeur et de détruire sa structure. [ 30 ]
Il est également possible d’utiliser les techniques suivantes:
- Administration intralésionnelle de stéroïdes. Cette méthode est relativement récente et n'est utilisée que depuis peu. Les injections permettent d'obtenir des résultats positifs sur les petits ostéoblastoclastomes: la tumeur diminue de taille. Parfois, à la fin du traitement, la lésion devient plus radio-opaque que la zone osseuse environnante.
- Introduction de l'interféron alpha. S'appuyant sur la théorie de l'origine vasculaire de l'ostéoblastoclastome, les spécialistes ont introduit l'injection d'interféron alpha. Ce médicament possède une action antiangiogénique, c'est-à-dire qu'il ralentit la croissance des vaisseaux sanguins. Cette méthode s'est avérée efficace chez environ 50 % des patients, mais son utilisation est relativement rare, en raison de nombreux effets secondaires, tels que maux de tête, détérioration générale de l'état de santé, fatigue intense et altération de la capacité de travail.
Le traitement de l'ostéoblastoclastome malin (primaire ou secondaire) repose exclusivement sur une intervention chirurgicale, comprenant la résection de la tumeur et de la zone osseuse. Une radiothérapie et une chimiothérapie sont prescrites avant et après l'opération.
Les ostéoclastomes inopérables (par exemple, certaines tumeurs sacrées et pelviennes) peuvent être traités par embolisation transcathéter de leur apport sanguin.
- Thérapie anti-RANKL
Les cellules géantes surexpriment un médiateur clé de l'ostéoclastogenèse: le récepteur RANK, lui-même stimulé par la cytokine RANKL, sécrétée par les cellules stromales. Des études sur le dénosumab, un anticorps monoclonal qui se lie spécifiquement à RANKL, ont donné des résultats thérapeutiques impressionnants, conduisant à son approbation par la Food and Drug Administration (FDA) américaine. [ 31 ], [ 32 ] Le dénosumab est principalement destiné aux patients présentant un risque élevé de récidive après une intervention chirurgicale initiale et une récidive locale.
Traitement chirurgical
Diverses études montrent que la résection large est associée à un risque réduit de récidive locale par rapport au curetage intralésionnel et peut augmenter la survie sans récidive de 84 % à 100 %.[ 33 ],[ 34 ],[ 35 ] Cependant, la résection large est associée à un taux plus élevé de complications chirurgicales et entraîne une déficience fonctionnelle, qui nécessite généralement une reconstruction.[ 36 ],[ 37 ],[ 38 ]
Si l'ostéoblastoclastome est localisé dans les os tubulaires longs, les interventions chirurgicales suivantes peuvent être utilisées:
- L'ablation marginale par alloplastie ou autoplastie est réalisée en cas d'ostéoblastoclastome bénin, à développement lent, à structure cellulaire et situé à la périphérie de l'épimétaphyse. Une fixation par vis métalliques est possible.
- Si le processus tumoral s'étend jusqu'au milieu diamétral de l'os, les 2/3 du condyle et une partie de la diaphyse avec la surface articulaire sont retirés. Le défaut est comblé par une allogreffe cartilagineuse. Des boulons et des vis solides sont utilisés. La connexion de l'allogreffe à la couche corticale de l'os hôte est réalisée obliquement afin d'éviter tout affaissement articulaire.
- En cas de destruction de l'épimétaphyse ou de fracture pathologique, une résection segmentaire avec désarticulation articulaire et remplacement du défaut par une allogreffe est réalisée. La fixation est assurée par une tige sur ciment.
- En cas de fracture pathologique et de malignité d'ostéoblastoclastome dans la partie proximale du fémur, une chirurgie de remplacement total de la hanche est réalisée.
- Lors de l'ablation des segments terminaux articulaires du genou, une greffe allo-hémiarticulaire avec fixation solide est utilisée. Une endoprothèse totale individuelle avec tige allongée en titane et une radiothérapie ultérieure sont possibles.
- Si la tumeur agressive est localisée à l'extrémité distale du tibia, une résection avec arthrodèse ostéoplasique de la cheville est réalisée. En cas de lésion du talus, une extirpation osseuse avec arthrodèse d'allongement selon Zatsepin est réalisée.
- Si le foyer pathologique est localisé au niveau du rachis cervical, un accès antérieur aux vertèbres est pratiqué. Un accès antérolatéral est possible en séparant soigneusement le pharynx et la face antérieure des vertèbres de la base du crâne.
- Au niveau de Th 1 -Th 2, une approche antérieure avec sternotomie oblique jusqu'au troisième espace intercostal est utilisée. Les vaisseaux sont soigneusement déplacés vers le bas. Si la lésion siège au niveau des vertèbres thoraciques 3 à 5, une approche antérolatérale et une résection de la troisième côte sont réalisées. L'omoplate est déplacée vers l'arrière sans sectionner les muscles. L'accès aux faces antérieures des vertèbres sacrées supérieures peut être difficile. Une approche rétropéritonéale antérolatérale droite est utilisée, avec une séparation soigneuse des vaisseaux et de l'uretère.
- Si une destruction sévère des vertèbres est détectée, ou si la tumeur s'est propagée aux arcades de la colonne thoracique et lombo-sacrée, une fixation transpédiculaire-translaminaire est réalisée avec ablation des vertèbres affectées et autoplastie.
- Si l'ostéoblastoclastome est localisé au niveau des os pubiens et ischiatiques, la zone affectée est retirée dans les limites des tissus sains, sans transplantation osseuse. Si la partie inférieure et le toit de l'acétabulum sont touchés, une ablation suivie d'une réparation ostéoplastique est indiquée.
- En cas de destruction du sacrum et de L5, les parties atteintes sont retirées postérieurement et stabilisées par fixation transpédiculaire. La tumeur est ensuite retirée par voie rétropéritonéale, suivie d'une greffe osseuse.
La prévention
Il n'existe pas de mesures préventives spécifiques pour prévenir l'apparition d'un ostéoblastoclastome. À titre préventif, les spécialistes recommandent un examen radiologique régulier tous les 1 à 2 ans afin de détecter et de traiter rapidement ces tumeurs.
Si une personne découvre une compaction osseuse, elle doit immédiatement consulter un médecin: un thérapeute, un orthopédiste, un oncologue, un traumatologue ou un vertébrologue.
Les recommandations médicales supplémentaires comprennent:
- éviter les blessures, les intoxications, manger correctement et de manière nutritive, être physiquement actif;
- consulter un médecin en temps opportun, notamment en ce qui concerne les maladies de l’appareil locomoteur;
- Assurez-vous de consulter un médecin et de subir un examen diagnostique si une nouvelle croissance d’origine inconnue apparaît.
Prévoir
Chez les patients atteints d'ostéoblastoclastome, l'évolution de la maladie dépend de nombreux facteurs, tels que les caractéristiques de l'évolution de la tumeur, sa malignité ou sa bénignité, sa localisation, sa propagation, la rapidité du traitement, etc. Ces dernières années, les résultats du traitement des tumeurs osseuses malignes ont considérablement progressé. Les médecins ont recours à une approche combinée, en recourant si nécessaire à une polychimiothérapie intensive. Parallèlement, le pourcentage de patients complètement guéris dépasse 70 %.
Les experts affirment que le pronostic est positif si l'ostéoblastoclastome est complètement retiré chirurgicalement et qu'il n'y a pas de récidive. Dans la mesure du possible, les chirurgiens s'efforcent toujours de réaliser des opérations conservatrices d'organes avec greffe osseuse simultanée. Ce n'est que dans certains cas qu'il s'agit d'interventions mutilantes, après lesquelles la personne ne peut plus effectuer certains actes: elle doit modifier son mode de vie. Dans de telles situations, les médecins entendent par « guérison » « l'absence de processus tumoraux ». Ces patients nécessitent ensuite une rééducation à long terme, un suivi orthopédique et parfois psychologique.

