Expert médical de l'article
Nouvelles publications
Causes et pathogénie de l'adénome de la prostate
Dernière revue: 04.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
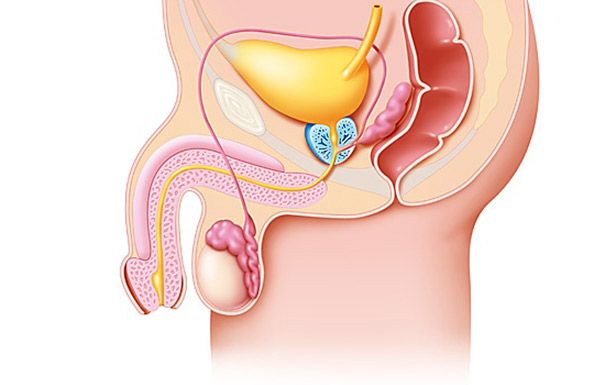
Il est impossible de comprendre la pathogenèse de l'adénome de la prostate sans prendre en compte les données modernes sur son anatomie et sa morphologie. La théorie moderne du développement de l'adénome de la prostate repose sur le concept zonal de la structure prostatique, selon lequel on distingue plusieurs zones de la prostate, qui diffèrent par les caractéristiques histologiques et fonctionnelles des éléments cellulaires qui les composent. Il s'agit des zones périphérique, centrale et transitoire, ainsi que de la zone du stroma fibromusculaire antérieur et du segment préprostatique.
Au niveau du tubercule séminal, les orifices de sortie du canal déférent s'ouvrent. La paroi de la partie proximale de l'urètre est constituée de fibres musculaires lisses longitudinales. Le sphincter préprostatique (génital), formé d'une épaisse couche de fibres musculaires lisses, entoure la partie proximale de l'urètre, du col de la vessie jusqu'au sommet du tubercule séminal, et prévient l'éjaculation rétrograde.
Des études histologiques ont montré que la croissance de l'adénome de la prostate (glande prostatique) débute dans les zones centrale et transitionnelle de la prostate. La zone transitionnelle de la prostate est constituée de deux glandes distinctes situées immédiatement derrière le sphincter interne de la vessie. Les canaux excréteurs de cette zone sont situés sur la paroi latérale de l'urètre, près du tubercule séminal. La zone transitionnelle proximale contient les glandes de la zone périurétrale; elles bordent le sphincter interne de la vessie et sont situées parallèlement à l'axe de l'urètre. Des ganglions adénomateux peuvent se développer aussi bien dans la zone transitionnelle que dans la zone para-urétrale. Outre l'hyperplasie nodulaire, la zone transitionnelle a tendance à croître avec l'âge.
La capsule prostatique joue un rôle important dans le développement des symptômes de l'adénome de la prostate (glande prostatique). Ainsi, chez le chien, la capsule prostatique est peu développée et, même en cas d'hyperplasie prononcée, les symptômes de la maladie se développent rarement. La capsule transmet la pression du tissu prostatique hypertrophié à l'urètre, provoquant une augmentation de la résistance urétrale.
Adénome de la prostate (glande prostatique): physiopathologie
La partie prostatique de l'urètre s'allonge et se déforme jusqu'à 4 à 6 cm ou plus, principalement en raison de la zone de la paroi postérieure située au-dessus du tubercule séminal. Le col vésical est surélevé et déformé, sa lumière prenant la forme d'une fente. De ce fait, la courbure naturelle de l'urètre s'accentue et, avec un développement irrégulier des lobes latéraux, l'urètre se courbe également transversalement, ce qui peut lui donner un aspect en zigzag. L'ouverture de la lumière du col vésical, due à une défaillance du mécanisme urétro-sphinctérien lors de la compensation détrusorienne, se manifeste cliniquement par une incontinence urinaire.
La vessie subit également de profondes modifications. Sa réaction à l'obstruction se déroule en trois étapes: irritabilité, compensation et décompensation. Au premier stade de l'obstruction infravésicale, la vessie réagit par une intensification des contractions du détrusor, permettant le maintien temporaire de l'équilibre fonctionnel et l'évacuation complète de l'urine. L'obstruction se développe ensuite et entraîne une hypertrophie compensatoire de la paroi vésicale, pouvant atteindre 2 à 3 cm d'épaisseur. Dans ce cas, elle peut prendre un aspect trabéculaire en raison de l'épaississement et du gonflement des faisceaux musculaires.
Le stade initial du développement trabéculaire est morphologiquement caractérisé par l'hypertrophie des cellules musculaires lisses. La progression du processus entraîne la séparation des éléments musculaires hypertrophiés et le remplissage des espaces inter-trabéculaires par du tissu conjonctif. Des dépressions, appelées faux diverticules, se forment entre les travées, dont les parois s'amincissent progressivement sous l'effet de la pression intravésicale accrue. Ces diverticules sont souvent multiples, atteignant parfois des tailles importantes.
Les propriétés élastiques du détrusor sont déterminées par la présence de collagène, qui représente 52 % de la quantité totale de protéines dans son tissu musculaire lisse. À mesure que les capacités compensatoires s'épuisent et que l'atrophie s'accentue, les parois de la vessie s'amincissent. Le détrusor perd sa capacité de contraction et d'étirement, ce qui entraîne une augmentation significative de la capacité de la vessie, atteignant 1 litre ou plus. Les modifications inflammatoires et trophiques concomitantes entraînent une sclérose prononcée de la couche musculaire de la paroi vésicale et une diminution de la teneur en collagène. La teneur en tissu conjonctif devient égale ou supérieure à celle des éléments musculaires.
Le degré de restauration de la structure normale de la paroi vésicale dépend de la durée de l'obstruction à l'écoulement urinaire. Une obstruction prolongée entraîne des modifications morphologiques irréversibles, entraînant des troubles fonctionnels prononcés de la vessie, impossibles à éliminer même par un traitement chirurgical. Une obstruction infravésicale sévère entraîne une augmentation de la pression vésicale, une altération de l'écoulement urinaire rénal et le développement d'un reflux vésico-urétéral et rénal, ainsi que d'une pyélonéphrite. Les uretères se dilatent, s'allongent, deviennent tortueux, une urétérohydronéphrose et une insuffisance rénale chronique se développent. La pathogénèse des modifications rénales et des voies urinaires supérieures chez les patients atteints d'adénome de la prostate est complexe et dépend de nombreux facteurs: modifications liées à l'âge, maladies concomitantes affectant la capacité fonctionnelle, développement d'une uropathie obstructive.
Au premier stade de l'uropathie obstructive, la préservation de l'appareil forniculaire des calices et l'intégrité de l'épithélium des tubules collecteurs des papilles préviennent l'apparition de reflux pelviens rénaux et la pénétration ascendante de l'infection dans le parenchyme rénal. À mesure que l'urétérohydronéphrose se développe, une déformation structurelle des voûtes calicielles se produit, créant des conditions favorables à l'apparition de reflux pelviens-tubulaires rénaux, puis pelviens-veineux et pelviens-lymphatiques.
En raison de l'augmentation de la pression intrapelvienne et du reflux pelvien-rénal, l'hémodynamique rénale est significativement altérée, suivie de modifications structurelles des artères intra-organiques, telles que leur oblitération et leur sténose diffuse. Ces troubles hémodynamiques entraînent d'importants changements métaboliques et une ischémie rénale sévère. L'uropathie obstructive entraîne une détérioration progressive de tous les indicateurs de l'état fonctionnel des reins. Ce processus se caractérise par une altération précoce de la capacité de concentration rénale, qui se manifeste principalement par une forte diminution de la réabsorption des ions Na et une augmentation de leur excrétion urinaire. Une altération de la fonction rénale au stade I de l'adénome de la prostate est observée chez 18 % des patients. Au stade II, une insuffisance rénale chronique complique l'évolution de la maladie chez 74 % des patients, dont 11 % en phase terminale. L'insuffisance rénale chronique est détectée chez tous les patients atteints d'adénome de la prostate de stade III, le stade intermittent étant observé chez 63 % et le stade terminal chez 25 % des personnes examinées.
L'infection urinaire joue un rôle fondamental dans la pathogenèse des troubles rénaux liés à l'adénome de la prostate et complique considérablement l'évolution de la maladie. La pyélonéphrite et l'insuffisance rénale sont responsables de jusqu'à 40 % des décès chez les patients atteints d'adénome de la prostate. Une pyélonéphrite chronique est observée dans 50 à 90 % des cas.
L'inflammation d'origine bactérienne survient principalement dans le tissu péritubulaire interstitiel. Dans la pathogénèse de la pyélonéphrite secondaire à l'adénome de la prostate, le rôle principal est joué par l'urostase, le développement d'un reflux vésico-urétéral et du bassinet rénal. L'infection pénètre dans le rein par voie ascendante depuis la vessie. Une infection urinaire accompagne la plupart des cas d'adénome de la prostate. Une cystite chronique a été observée chez 57 à 61 % des patients ambulatoires et 85 à 92 % des patients hospitalisés. À cet égard, la pathogénèse de la pyélonéphrite chronique chez les patients atteints d'adénome de la prostate peut être représentée comme suit: obstruction sous-vésicale → dysfonctionnement vésical → cystite → insuffisance des jonctions vésico-urétérales → reflux vésico-urétéral → pyélonéphrite chronique.
La présence d'un processus inflammatoire concomitant au niveau de la prostate joue un rôle important dans la formation du tableau clinique de l'adénome prostatique. La fréquence de la prostatite chronique associée à l'adénome prostatique, selon les données de laboratoire, chirurgicales et d'autopsie, est respectivement de 73 %, 55,5 % et 70 %. La stase veineuse, la compression des canaux excréteurs des acini par le tissu hyperplasique de la glande et son œdème sont des conditions préalables au développement d'une inflammation chronique. L'examen morphologique du matériel chirurgical a montré que, dans la plupart des cas, le processus inflammatoire était localisé à la périphérie de la glande. Une prostatite chronique concomitante peut se manifester cliniquement par une dysurie, nécessitant un diagnostic différentiel avec les troubles urinaires causés par l'adénome prostatique lui-même. Sa présence entraîne également une augmentation du nombre de complications postopératoires précoces et tardives, nécessitant des mesures pour identifier et traiter la prostatite chronique au stade du traitement conservateur ou de la préparation à la chirurgie.
Les calculs vésicaux dans l'adénome se forment secondairement en raison de troubles de la vidange vésicale. Ils sont détectés chez 11,7 à 12,8 % des patients. Ils ont généralement une forme ronde régulière, peuvent être uniques ou multiples, et leur composition chimique est composée d'urates ou de phosphates. Les calculs rénaux accompagnent l'adénome de la prostate dans 3,6 à 6,0 % des cas.
Une complication fréquente de l'adénome de la prostate est la rétention urinaire aiguë complète, qui peut se développer à n'importe quel stade de la maladie. Dans certains cas, il s'agit de l'aboutissement du processus obstructif associé à une décompensation de la contractilité du détrusor, tandis que dans d'autres cas, elle apparaît soudainement sur fond de symptômes modérés de troubles urinaires. Il s'agit souvent de la première manifestation clinique de l'adénome de la prostate. Selon la littérature, cette complication est observée chez 10 à 50 % des patients, le plus souvent au stade II de la maladie. Les facteurs favorisant le développement de cette complication peuvent être une mauvaise alimentation (consommation d'alcool, d'épices), l'hypothermie, la constipation, une vidange intempestive de la vessie, le stress, la prise de certains médicaments (anticholinergiques, tranquillisants, antidépresseurs, diurétiques).
Les principaux facteurs de développement de la rétention urinaire aiguë sont la croissance de tissu hyperplasique, les modifications fonctionnelles du tonus du cou et des muscles de la vessie et une altération de la microcirculation des organes pelviens avec le développement d'un œdème de la prostate.
Au stade initial de la rétention urinaire aiguë, l'augmentation de l'activité contractile du détrusor entraîne une augmentation de la pression intravésicale. Aux stades suivants, en raison de l'étirement de la paroi vésicale et d'une diminution de sa capacité contractile, la pression intravésicale chute.

