Expert médical de l'article
Nouvelles publications
Virus d'Epstein-Barr
Dernière revue: 04.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
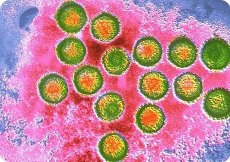
Le virus d'Epstein-Barr (VEB) est responsable de la mononucléose infectieuse, qui touche des personnes de tous âges, ainsi que d'une tumeur de la mâchoire supérieure, le lymphome de Burkitt, observé chez les enfants et les adolescents en Afrique centrale, et d'un carcinome nasopharyngé chez les hommes adultes en Chine. Le virus d'Epstein-Barr a été identifié pour la première fois par microscopie électronique de cellules transplantées issues du lymphome de Burkitt.
Le virus d'Epstein-Barr diffère considérablement des autres herpèsvirus par ses propriétés antigéniques. Différents antigènes sont détectés par CSC, immunodiffusion et RIF. Les plus précoces sont l'antigène membranaire (MA ou LYDMA: antigène membranaire, ou antigène membranaire détecté par les lymphocytes), l'antigène nucléaire fixateur du complément (EBNA – antigène nucléique d'Epstein-Barr); l'antigène tardif est l'antigène de capside virale (VCA – antigène de capside virale).
Le virus d'Epstein-Barr est assez original dans son interaction avec la cellule hôte qu'il infecte: il provoque non pas la mort, mais la prolifération des lymphocytes. La transformation des lymphocytes provoquée par le virus d'Epstein-Barr permet à ces derniers d'être cultivés pendant une longue période; dans ce cas, un test RIF positif avec un antisérum anti-virus d'Epstein-Barr est détecté. Cette transformation rend les lymphocytes capables de se diviser à l'infini. Les génomes du virus d'Epstein-Barr apparaissent en grande quantité dans toutes les cellules, et l'antigène nucléaire (EBNA) est libéré dans l'environnement.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
Pathogénèse et symptômes de la mononucléose infectieuse
La pathogénèse de l'infection causée par le virus d'Epstein-Barr est encore mal comprise. Dans la mononucléose infectieuse, le virus d'Epstein-Barr pénètre dans la muqueuse buccale et nasopharyngée, puis dans les ganglions lymphatiques régionaux, se multiplie et se dissémine par voie hématogène. Dans les ganglions lymphatiques, les amygdales et la rate, les cellules réticulaires et lymphoïdes prolifèrent pour former de grandes formes mononucléaires; une nécrose focale est fréquente. Des infiltrats de cellules lymphoïdes peuvent se former dans le foie.
La période d'incubation de la mononucléose infectieuse est de 4 à 60 jours, le plus souvent de 7 à 10 jours. La maladie se caractérise par une évolution progressive: élévation de la température, apparition de maux de gorge, altération de la respiration nasale, augmentation du volume des ganglions lymphatiques régionaux et apparition de plaques sur les amygdales. Une leucocytose est observée dans le sang. L'un des signes les plus caractéristiques de la maladie est l'apparition de cellules mononucléaires matures atypiques de taille moyenne à grande, avec un protoplasme basophile large – cellules mononucléaires atypiques et lymphocytes à plasma large; leur nombre est de 10 à 15 % ou plus. Les complications (sinusite, pneumonie, méningite, néphrite) sont rares, et le pronostic est favorable. L'immunité est très spécifique. Les lymphocytes B produisent des particules virales, mais la malignité est généralement absente. Ceci est associé à l'apparition de lymphocytes T tueurs spécifiques, dont la cible est l'antigène viral MA à la surface des lymphocytes B. Les cellules tueuses naturelles et le mécanisme des cellules K sont activés. L'activité des suppresseurs augmente, inhibant la prolifération et la différenciation des lymphocytes B et empêchant ainsi la reproduction des cellules affectées. Lors de la guérison, des lymphocytes T mémoires apparaissent, qui détruisent les lymphocytes B infectés par le virus après leur restimulation. Ces cellules circulent dans le sang des personnes guéries à vie. Des anticorps neutralisant le virus sont également synthétisés. Dans le lymphome de Burkitt et le carcinome du nasopharynx, les cellules affectées contiennent de multiples copies du génome intégré du virus d'Epstein-Barr, et l'antigène EBNA apparaît dans les noyaux cellulaires. Des anticorps dirigés contre l'antigène de capside, d'abord de classe IgM, puis de classe IgG, apparaissent dans le sang des personnes guéries. Plus tard, des anticorps dirigés contre les antigènes précoces MA et EBNA apparaissent. Ces anticorps persistent à vie. Pour détecter l'ADN viral dans les cellules transformées affectées, la méthode de la sonde ADN est utilisée.

