Expert médical de l'article
Nouvelles publications
HPV de type 33: symptômes, traitement
Dernière revue: 04.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
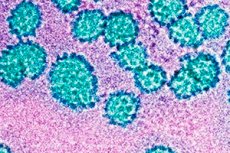
Aujourd'hui, en médecine, on observe de plus en plus de diagnostics et d'abréviations incompréhensibles, qui effraient les personnes simples et peu informées. Le diagnostic de « VPH de type 33 » en est un exemple frappant. Quel est ce diagnostic étrange? Examinons-le plus en détail.
Qu'est-ce que c'est?
De nombreuses personnes doivent subir des analyses de laboratoire. Après avoir reçu les résultats, on peut lire un diagnostic aussi effrayant dans une analyse de sang. La première question qui vient à l'esprit est: qu'est-ce que c'est? En d'autres termes, cette abréviation peut être appelée « virus du papillome humain ». Le code de la souche est indiqué à côté: 33. Ce virus est assez fréquent chez les personnes d'origine caucasienne.
Le virus du papillome humain (VPH) 33, un membre du groupe alpha-9, est responsable d'environ 5 % des cas de cancer du col de l'utérus dans le monde.[ 1 ],[ 2 ]
Structure HPV de type 33
La structure du virus est très spécifique. Il convient tout d'abord de noter que sa taille peut varier dans une fourchette assez large, de 100 à 200 nm. La membrane est constituée de deux couches. La première est constituée de lipides, la seconde d'un complexe de glycoprotéines. Les composants sont reliés entre eux par des liaisons non covalentes.
Génotypes 33 du VPH à haut risque
Le papillomavirus appartient à la famille des Papillomaviridae. Il s'agit d'un vaste groupe de virus responsables de tumeurs.
Vingt-huit variantes du HPV33 ont été identifiées, qui formaient cinq groupes phylogénétiques: les lignées A1, A2 et B (sous-) précédemment identifiées et les nouvelles lignées A3 et C (sous-).
Les variants du VPH33 ont été classés en deux lignées principales, A et B. La lignée A a été subdivisée en deux sous-lignées, A1, qui comprend la séquence prototype [M12732.1 (Cole et Streeck, 1986) [ 3 ], et A2. Cette classification repose sur la constatation que la séquence génomique complète d'une lignée variante majeure diffère d'environ 1,0 % de celle d'une autre lignée variante du même type de VPH, avec des différences de 0,5 à 0,9 % définissant les sous-lignées (Chen et al., 2011). [ 4 ]
Français Les sous-lignées A1 sont distribuées dans le monde entier, bien que la fréquence relative varie selon la région. Les sous-lignées A2 ont été rarement détectées en Afrique et en Amérique du Sud, tandis que la lignée B est spécifique à l'Afrique. Les sous-lignées C ont été trouvées uniquement dans des échantillons provenant d'Afrique, et les sous-lignées A3 étaient spécifiques à l'Asie/Océanie, ce qui est soutenu par deux rapports supplémentaires de Chine ( Wu et al., 2009 ) [ 5 ] et du Japon [basé sur E6 uniquement ( Xin et al., 2001 )]. [ 6 ] Cependant, la rareté observée des lignées A3 et C doit être prise en compte lors de l'interprétation de ces résultats.
ADN du VPH 33
Le composant principal est constitué par les gènes oncogènes, qui comprennent des composants protéiques. Ils véhiculent des informations susceptibles de déclencher la croissance tumorale. L'ADN du VPH 33 est formé de deux spirales, ce qui renforce les propriétés du virus. Un rôle important est également attribué aux gènes cellulaires régulateurs, qui régulent les principaux processus cellulaires et facteurs de transformation.
Cycle de vie HPV de type 33
La vie d’un virus est cyclique et se déroule en plusieurs étapes.
Au premier stade, le virus est absorbé par les récepteurs de la cellule hôte. Ce processus est rendu possible grâce à la présence de glycoprotéines dans le complexe membranaire et dans les virions eux-mêmes.
La deuxième étape est caractérisée par la pénétration active du virus directement dans la structure cellulaire de l'hôte. Cela déclenche les principaux mécanismes d'interaction du virus avec la matrice cellulaire. Il existe différents mécanismes d'interaction.
Au cours de la troisième étape, le virus se déplace dans la cellule, formant des bulles qui le protègent temporairement. Le point final du transport viral est l'atteinte des ribosomes et du réticulum endoplasmique. Parfois, les particules virales et les virus eux-mêmes migrent vers le noyau.
La quatrième étape peut être décrite comme le processus de déshabillage du virion. Ce processus repose essentiellement sur la déprotéinisation et la libération de la supercapside et des capsides.
Au cinquième stade, le virion se dissout complètement et le processus de synthèse des virus commence, qui détruisent ensuite la cellule et sont libérés à l'extérieur.
Au sixième stade, le virion est assemblé et la nucléocapside est formée. Le processus d'auto-assemblage des particules virales est lancé.
Au septième stade, les particules virales quittent la cellule. Débute alors la phase active de l'infection, sa progression.
Ensuite, le cycle de vie se répète, de nouvelles cellules sont impliquées et, en conséquence, la maladie se développe et progresse.
Pathogénèse
Le VPH se transmet principalement par contact cutané. Des études épidémiologiques indiquent clairement que le risque de contracter une infection génitale au VPH et un cancer du col de l'utérus est lié à l'activité sexuelle. Le VPH est très résistant à la chaleur et à la sécheresse, et une transmission asexuée peut également se produire, par exemple par contact prolongé avec des vêtements contaminés partagés [ 7 ]. Une personne est plus à risque de contracter le VPH si elle a eu plusieurs partenaires sexuels à un moment donné ou si elle est le partenaire d'une personne ayant eu plusieurs partenaires sexuels. Une activité sexuelle précoce augmente également le risque, tout comme des antécédents d'autres maladies sexuellement transmissibles, de verrues génitales, de tests Pap anormaux ou de cancer du col de l'utérus ou du pénis chez la personne ou un partenaire sexuel. L'utilisation de préservatifs peut ne pas protéger adéquatement contre l'exposition au VPH, car le VPH peut se transmettre par contact avec des tissus labiaux, scrotaux ou anaux infectés qui ne sont pas protégés par un préservatif.
Outre l'activité sexuelle, l'âge est un facteur de risque important d'infection par le VPH [ 8 ]. L'activité métaplasique la plus élevée est observée pendant la puberté et la première grossesse et diminue après la ménopause. L'infection par le VPH est plus fréquente chez les jeunes femmes sexuellement actives âgées de 18 à 30 ans. La prévalence diminue fortement après 30 ans. Cependant, le cancer du col de l'utérus est plus fréquent chez les femmes de plus de 35 ans, ce qui suggère une infection à un âge plus jeune et un développement lent du cancer.
La principale réponse immunitaire à l'infection par le VPH est à médiation cellulaire; par conséquent, les conditions qui altèrent l'immunité à médiation cellulaire, telles que la transplantation rénale ou les maladies virales humaines, augmentent le risque d'acquisition et de progression du VPH.[ 9 ],[ 10 ]
L'immunosuppression locale causée par le tabagisme et l'activité mutagène des composants de la cigarette ont été démontrées dans les cellules cervicales et peuvent favoriser la persistance du VPH ou une transformation maligne similaire à celle observée dans les poumons.[ 11 ],[ 12 ] Dans l'ensemble, savoir comment le VPH 33 est transmis peut aider à prévenir l'infection.
Symptômes
Il existe plusieurs formes de la maladie. Les symptômes varient selon les cas. Dans la forme génitale, les muqueuses des organes génitaux et de l'appareil reproducteur sont endommagées. Douleurs, démangeaisons, brûlures et irritations apparaissent. Les symptômes ressemblent souvent à ceux du muguet: des pertes blanches, parfois cassantes, apparaissent. Des verrues, des excroissances et des papillomes apparaissent souvent directement sur les muqueuses du vagin, du col de l'utérus et de l'utérus.
Dans la forme cutanée, des excroissances et des papillomes peuvent apparaître. Ils sont principalement localisés sur la couche supérieure de la peau, l'épiderme. Ils peuvent être plats ou surélevés. Il est également important de noter que les verrues peuvent croître et se multiplier assez rapidement. Elles peuvent être uniques ou multiples. Souvent, les verrues constituent la seule manifestation de cette maladie.
L’infection au VPH sexuellement transmissible entraîne l’une des trois issues possibles.
- La première est celle des verrues anogénitales (condylomes acuminés) situées sur ou autour des organes génitaux et de l’anus, chez les hommes comme chez les femmes.
- Le deuxième résultat est une infection latente ou inactive, où peu de personnes savent qu'elles sont infectées car les symptômes visibles sont rares et la zone infectée reste cytologiquement normale. L'ADN du VPH est présent chez environ 10 % des femmes dont l'épithélium cervical est cytologiquement normal.
- Le troisième résultat est l'infection active, associée aux types de VPH à haut risque. Le virus provoque des modifications des cellules infectées pouvant entraîner une néoplasie intraépithéliale du pénis, de l'urètre, du vagin, de la vulve ou du col de l'utérus. Les types de VPH à haut risque comprennent les types associés au cancer du col de l'utérus et les types définis comme à risque intermédiaire, moins fréquemment représentés dans les cancers. Ces infections peuvent entraîner un cancer du col de l'utérus. Des études prospectives ont montré que 15 à 28 % des femmes positives à l'ADN du VPH ont développé une SIL dans les deux ans, contre seulement 1 à 3 % des femmes négatives à l'ADN du VPH.
Papillomes
Elle ressemble à une verrue, ou à une petite masse qui s'élève sur une tige. Cette structure est représentée par du tissu conjonctif. Elle est recouverte d'un épithélium multicouche. Elle peut s'élever fortement au-dessus de la surface (sur une tige) sur laquelle elle pousse, et peut aussi être plate et s'étendre horizontalement.
Le taux de croissance est assez faible, ce qui est dû à la croissance lente des tumeurs. Le danger réside dans les tumeurs situées sur les organes internes: elles peuvent être endommagées et provoquer des saignements. Lorsqu'elles sont localisées dans la lumière des organes internes (larynx, œsophage, intestins), elles peuvent se développer et obstruer la lumière. Cela entraîne les pathologies associées: suffocation, obstruction. Ces tumeurs doivent être retirées. Le principal traitement du papillome est la chirurgie, qui consiste en son excision.
HPV 33 chez les hommes
Les hommes sont souvent porteurs de ce virus, mais la maladie ne se manifeste pas chez eux. Le virus peut persister dans le sang sous une forme inactive ou être simplement inhibé par le système immunitaire. Cependant, au contact d'une femme, celle-ci est souvent infectée, car son immunité est bien plus faible et ne lui permet pas de résister pleinement à l'infection.
La principale manifestation est la formation de papillomes (multiples, uniques). Pour traiter le VPH 33 chez l'homme, on utilise des médicaments, des plantes médicinales et des préparations homéopathiques.
HPV 33 chez les femmes
Les femmes sont plus souvent atteintes par ce virus. Dans ce cas, la forme génitale de la maladie prédomine. Elle se manifeste le plus souvent par des papillomes et des condillomes situés sur la muqueuse génitale. Le risque réside dans le risque de dégénérescence maligne de ces néoplasmes, leur transformation en tumeur maligne. Il est à noter que souvent, la seule façon de les traiter est l'excision chirurgicale. Cependant, un traitement complémentaire est nécessaire pour prévenir les récidives et la récidive.
HPV 33 et dysplasie modérée
Leur particularité réside dans leur potentiel oncogène, c'est-à-dire qu'ils provoquent le développement de tumeurs malignes dans certaines conditions: immunité réduite, réactivité et sensibilisation accrues, faiblesse, diminution de l'endurance et de la résistance de l'organisme, perturbation du cycle biochimique, de l'état structurel et fonctionnel normal de l'organisme, ainsi que déséquilibre hormonal. Dans ces conditions, des papillomes, des fibromes, des myomes, des fibromyomes et des excroissances fibreuses se développent. Il s'agit d'une dysplasie modérée, directement liée au VPH 33. Cette affection peut être qualifiée de pré-cancer. Il existe toujours un risque potentiel de progression de ces affections et de leur transformation en tumeurs malignes – sarcomes, cancers, leucémies.
HPV 33 et grossesse
L'apparition du VPH 33 pendant la grossesse est un mauvais signe, car ce virus peut entraîner des pathologies liées à la grossesse. Il peut s'agir d'avortements spontanés, de fausses couches, de naissances prématurées ou de mortinaissances. Les enfants présentent souvent des anomalies du développement: malformations physiques, diverses anomalies mentales et fonctionnelles, ainsi qu'un retard mental (RM), un retard mental, des troubles de la parole et du développement affectif.
Il s'agit de cas extrêmes, caractérisés par une forte concentration virale et une charge virale élevée. Autrement, avec un traitement et une surveillance médicale constante, la grossesse peut se dérouler normalement. Cependant, il existe toujours un risque d'infection génito-urinaire et de saignement, particulièrement aggravé lors de l'accouchement. Le risque d'infection de l'enfant est accru pendant l'accouchement.
Diagnostics
Vous aurez besoin d'un virologue ou d'un immunologiste expérimenté. Vous pouvez également contacter un infectiologue, un biologiste, un biochimiste ou un bactériologiste. Si la clinique ne dispose pas de tels spécialistes, vous devez contacter le thérapeute du service concerné; il vous orientera vers le spécialiste approprié ou vous prescrira simplement les examens nécessaires. La principale méthode de confirmation du diagnostic est la confirmation directe de la présence du virus dans le sang, ce qui ne peut être obtenu qu'en effectuant les tests appropriés. Des analyses de laboratoire sont utilisées (ce sont les seules méthodes de recherche efficaces et fiables).
Dans la plupart des cas, le matériel d'étude est du sang. Des méthodes virologiques et sérologiques sont prescrites pour détecter le virus lui-même dans le sang, ses produits de son activité vitale ou ses fragments d'ADN. Le laboratoire utilise diverses méthodes d'analyse. Cependant, pour détecter le virus, il est conseillé d'utiliser la méthode PCR, ou séquençage de l'ADN, qui permet de détecter le virus lui-même dans le sang, et non les anticorps, en réaction du système immunitaire à son introduction.
Les tests PCR spécifiques de type reposent sur les variations de séquence présentes dans les gènes E6 et E7 des sous-types de VPH. Quatorze tests PCR spécifiques de type pour les types de VPH à haut risque (VPH-16, -18, -31, -33, -35, -39, -45, -51, -52, -56, -58, -59, -66 et -68) ciblent environ 100 pb dans l'ORF E7. [ 13 ]
Le génome est composé de plus de 100 000 nucléotides et de 9 gènes. Sa surface interne est recouverte d'une matrice, formée des protéines p17/18. Le génome est également composé de 3 gènes de structure et de 6 gènes de régulation. Il convient également de noter que le virus est très variable, notamment par rapport à d'autres virus. Plusieurs chercheurs travaillent encore au décodage de l'ADN du VPH de type 33.
La méthode ELISA (dosage immuno-enzymatique) n'est pas informative, car elle réagit à la quantité de complexe antigène-anticorps. De plus, les anticorps persistent toute la vie après une seule maladie. Il est donc impossible de tirer des conclusions sur le stade et le degré d'activité de l'infection virale dans l'organisme.
L'examen médical est également important. Il procédera à un examen complet et établira un diagnostic. Un examen visuel permettra au médecin de suspecter la présence du VPH de type 33, car il se manifeste par des signes spécifiques. Mais pour confirmer définitivement la maladie, il est important non seulement de poser un diagnostic, mais aussi d'établir un diagnostic différentiel. Cela signifie que les symptômes doivent être différenciés de ceux d'autres cas et manifestations similaires.
D'autres méthodes peuvent inclure un examen microscopique et un grattage. Selon la gravité de la pathologie, un immunogramme, des analyses cliniques et biochimiques sanguines et urinaires, ainsi que des tests de dysbactériose peuvent être nécessaires.
La microscopie permet d'identifier le virus lui-même ou ses déchets dans un frottis et d'en examiner les caractéristiques spécifiques. Ces données permettent de déterminer la position systématique précise de l'agent pathogène, jusqu'à son espèce et son genre. Plus cette identification est précise, plus le choix du traitement sera précis et efficace. Il est également important d'obtenir des indicateurs quantitatifs, car le plan de traitement ultérieur et son efficacité dépendent de la quantité de virus dans le sang (charge virale).
La principale méthode de détection du VPH à haut risque reste le test Pap (FAP). Ce test doit son nom au pathologiste George Papanicolaou, qui l'a introduit en 1949, avant que la cause du cancer du col de l'utérus ne soit connue. Depuis son introduction, le frottis a contribué à réduire l'incidence et la mortalité du cancer du col de l'utérus de moitié à deux tiers environ. [ 14 ] Le frottis est un outil de dépistage qui recherche les modifications des cellules de la zone de transformation du col de l'utérus. Ces modifications sont souvent causées par le VPH.
Norme HPV 33
D'un point de vue médical et biologique, l'absence totale de virus dans le sang est considérée comme la norme. Il s'agit toutefois d'un cas idéal, extrêmement rare dans le contexte de la vie moderne. Il existe donc des normes conditionnelles de présence du VPH 33 dans l'organisme. Cependant, elles varient considérablement d'un pays à l'autre. Seuls quelques pays considèrent l'absence totale de virus dans le sang comme la norme.
Traitement
Le traitement consiste principalement en l'excision chirurgicale des néoplasmes. Aujourd'hui, outre la chirurgie traditionnelle, il existe de nombreuses méthodes pour éliminer les papillomes. Les plus efficaces sont le laser, la cryothérapie, les ondes radio et la radiofréquence, l'électrocoagulation, l'élimination thermique et électrothermique des papillomes. Il existe également des méthodes chimiques pour éliminer les papillomes.
La plupart des changements induits par le VPH dans les cellules cervicales sont transitoires et 90 % régressent spontanément dans les 12 à 36 mois, à mesure que le système immunitaire élimine le virus.[ 15 ]
Traditionnellement, on a recours à un traitement antiviral. Parmi les médicaments classiques, on trouve l'inosiplex, l'interféron, l'amixine, la cycloférone et la podophylline. La podophylline, un agent cytotoxique qui arrête la mitose en métaphase (également utilisé pour traiter les verrues génitales), est associée à la vidarabine, un inhibiteur de l'ADN polymérase qui inhibe l'expression des gènes du VPH et la croissance cellulaire dans les lignées cellulaires du cancer du col de l'utérus. [ 16 ]
L'IFN et le 5-fluorouracile intravaginal ont montré des réponses variables lors d'études cliniques et in vitro. L'IFN-α est approuvé pour le traitement des verrues génitales. Les effets de l'IFN-α, de l'IFN-β et de l'IFN-γ ont été étudiés sur plusieurs lignées cellulaires de carcinomes humains.[ 17 ]
Il est important d'effectuer un traitement immunomodulateur visant à normaliser l'immunité. Un traitement immunostimulant, visant à renforcer l'immunité, est généralement nécessaire. Ainsi, le système immunitaire résiste de manière autonome à l'infection, sa résistance et son endurance augmentent, et le virus est inhibé.
Le traitement traditionnel est utilisé à des fins de prévention, de récupération postopératoire ou simplement comme moyen efficace de réduire la microflore et la charge virale. Il peut s'agir de médicaments, de divers moyens physiothérapeutiques, de médecine traditionnelle, d'homéopathie et de phytothérapie. Des vaccinations antivirales préventives sont également pratiquées, ce qui contribue à prévenir la dégénérescence maligne des cellules. En cas de formation de condillomes et de papillomes, leur cautérisation et leur brûlure sont souvent pratiquées.
Que faire si le VPH 33 est détecté?
Tout d'abord, vous devez consulter un médecin qui choisira le traitement approprié. Plus le traitement est commencé tôt, plus il sera efficace. Le médecin, en fonction des résultats des analyses de laboratoire et instrumentales, vous indiquera la marche à suivre. Si le VPH 33 est détecté, un traitement médicamenteux ou chirurgical (excision du papillome) peut être nécessaire. Un traitement antiviral et immunostimulant est également utilisé.
Est-il possible de guérir le VPH 33?
Cette pathologie répond bien au traitement si le système immunitaire est normal. Ainsi, si le système immunitaire est affaibli, diverses exacerbations, maladies et rechutes peuvent être observées. Le danger réside dans le potentiel oncogène du virus. Si le système immunitaire est normal, le virus peut simplement persister dans le sang sans provoquer d'exacerbation de l'infection.
Il est donc impossible de répondre clairement à la question: « Est-il possible de guérir le VPH 33? ». Il est donc important de maintenir un niveau d'immunité normal. Évitez le surmenage et le stress. Un traitement antiviral, une stimulation du système immunitaire ou une vitaminothérapie peuvent rendre le virus inactif. Il persistera alors dans le sang sans provoquer de maladie aiguë. Cependant, il est quasiment impossible d'éliminer complètement le virus du sang: une personne reste porteuse du virus et peut infecter d'autres personnes.
Prévention HPV de type 33
La prévention repose sur le respect des règles d'hygiène, une vie sexuelle adéquate (avoir un partenaire régulier, utiliser une protection lors des contacts avec des partenaires temporaires, un traitement préventif si un partenaire sexuel a une infection. Ce sont les principales mesures préventives de base. Il est également important de maintenir un système immunitaire normal - consultez périodiquement un immunologiste, faites-vous tester pour les virus, les infections latentes, suivez des cures de vitamines et, si nécessaire, des immunostimulants.
Il est important de bien manger, d'intégrer la quantité nécessaire de vitamines et de minéraux dans son alimentation, de se soumettre à des examens préventifs réguliers et, si nécessaire, de suivre un traitement rapide. Maintenir un niveau élevé d'immunité est particulièrement important, car le développement de la maladie n'est possible qu'en cas d'immunité réduite et de microflore altérée.
Les principales approches de prévention de l'infection par le VPH comprennent la réduction des risques et le développement de vaccins contre le VPH. L'utilisation de préservatifs en latex et de spermicides peut réduire le risque d'infection par le VPH. Cependant, les préservatifs ne sont pas totalement fiables, car le VPH peut se transmettre par contact avec d'autres parties du corps, comme les lèvres, le scrotum ou l'anus, qui ne sont pas protégées par un préservatif.
Français Une étude de phase I, en double aveugle, randomisée et contrôlée par placebo, portant sur l'innocuité et l'immunogénicité, a été menée en utilisant un vaccin sous-unitaire constitué d'une VLP générée à partir de la totalité de la protéine de capside majeure L1 de la souche 114K du VPH-16 [ 18 ]. Le vaccin a été produit en insérant le gène de la capside L1 dans un vecteur baculovirus. Le gène a ensuite été exprimé dans des cellules d'insecte Sf9 transfectées. Une dose optimale de 50 μg de vaccin VLP L1 contre le VPH-16 a été administrée par injection dans le muscle deltoïde à 0, 1 et 4 mois. Le vaccin a généré des titres élevés d'anticorps neutralisants spécifiques du type sans adjuvant et a été bien toléré.
Depuis 2017, Gardasil 9® est le seul vaccin contre le VPH disponible aux États-Unis. D'autres vaccins contre le VPH sont disponibles hors des États-Unis. Gardasil 9 aide à prévenir l'infection par quatre types de VPH (16, 18, 6 et 11) et cinq autres types à haut risque: 31, 33, 45, 52 et 58. Ensemble, ces types sont responsables d'environ 90 % des cancers du col de l'utérus.
Recommandations de l’American Cancer Society pour l’utilisation du vaccin contre le VPH.
- La vaccination systématique contre le VPH pour les filles et les garçons devrait commencer à l'âge de 11-12 ans. La série vaccinale peut être commencée dès l'âge de 9 ans.
- La vaccination contre le VPH est également recommandée pour les femmes de 13 à 26 ans et pour les hommes de 13 à 21 ans qui n'ont pas encore commencé leur série vaccinale ou qui l'ont commencée mais pas terminée. Les hommes de 22 à 26 ans peuvent également être vaccinés.
- La vaccination contre le VPH est également recommandée à l’âge de 26 ans pour les hommes ayant des rapports sexuels avec des hommes et pour les personnes dont le système immunitaire est affaibli (y compris les personnes infectées par le VIH) si elles n’ont pas été vaccinées auparavant.
- Pour les personnes âgées de 22 à 26 ans qui n’ont pas encore commencé la vaccination ou qui ont commencé mais pas terminé la série, il est important de savoir que la vaccination à un âge plus avancé est moins efficace pour réduire le risque de cancer.
Prévoir
Dans la plupart des cas, avec un traitement approprié et rapide, le pronostic sera favorable. Le VPH de type 33 est assez facile à éliminer. L'essentiel est de maintenir une immunité normale et de suivre toutes les recommandations du médecin. Si des papillomes apparaissent, leur ablation chirurgicale (excision) peut être nécessaire. Il s'agit d'une intervention rapide et indolore qui ne nécessite pratiquement aucune convalescence. Le traitement antiviral joue un rôle important. En l'absence de traitement, des complications peuvent survenir, dont la plus dangereuse est le développement de tumeurs malignes.

