Expert médical de l'article
Nouvelles publications
Fibroélastose
Dernière revue: 05.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
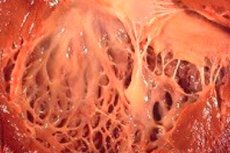
En médecine, le terme « fibroélastose » désigne les modifications du tissu conjonctif recouvrant la surface des organes internes et des vaisseaux sanguins, causées par une perturbation de la croissance des fibres élastiques. Parallèlement, on observe un épaississement des parois des organes et de leurs structures, ce qui affecte nécessairement le fonctionnement des systèmes vitaux, notamment les systèmes cardiovasculaire et respiratoire. Ceci entraîne une détérioration du bien-être du patient, notamment lors d'un effort physique, affectant sa qualité et sa longévité.
Épidémiologie
En général, les maladies accompagnées de modifications du tissu conjonctif, entraînant un épaississement des membranes et des parois des organes internes, peuvent être divisées en deux groupes: la fibroélastose cardiaque et la fibroélastose pulmonaire. La pathologie cardiaque peut être congénitale ou acquise; dans la forme pulmonaire, on parle de maladie acquise.
La fibroélastose pulmonaire commence à se développer à l'âge mûr (vers 55-57 ans), bien que dans la moitié des cas, son origine doive être recherchée dès l'enfance. Une période « légère » est caractéristique, pendant laquelle les symptômes sont absents. Par ailleurs, la maladie ne présente aucune préférence de genre et peut toucher aussi bien les femmes que les hommes. Cette pathologie plutôt rare se caractérise par des modifications des tissus de la plèvre et du parenchyme pulmonaire (cellules fonctionnelles), principalement dans le lobe supérieur. L'étiologie et la pathogénèse de la maladie restant obscures, elle est classée comme une pathologie idiopathique. Selon la terminologie médicale, on parle de « fibroélastose pleuroparenchymateuse ». [ 1 ]
La fibroélastose cardiaque est le terme générique désignant une pathologie des membranes cardiaques, caractérisée par leur épaississement et leur diminution de fonctionnalité. Les formes congénitales de cette pathologie se caractérisent par un épaississement diffus (généralisé) de la membrane interne du cœur. Il s'agit d'un fin tissu conjonctif tapissant la cavité cardiaque (ses sections) et formant ses valvules.
Chez les patients adultes, une forme focale de la maladie est généralement diagnostiquée, lorsque la surface interne du cœur semble être recouverte de plaques de tissu plus résistant et plus épais (elle peut inclure non seulement des fibres envahissantes, mais également des masses thrombotiques).
Dans la moitié des cas de fibroélastose cardiaque, non seulement la paroi de l'organe s'épaissit, mais aussi les valvules (mitrale bicuspide entre l'oreillette et le ventricule du même nom, aortique tricuspide entre le ventricule gauche et l'aorte, pulmonaire entre le ventricule droit et l'artère pulmonaire). Ceci peut perturber le fonctionnement des valvules et provoquer un rétrécissement de l'orifice artériel, déjà petit par rapport aux autres cavités cardiaques.
En terminologie médicale, la fibroélastose endocardique est appelée fibroélastose endocardique (fibroélastose prénatale, sclérose endocardique, endocardite fœtale, etc.). Cependant, la couche musculaire moyenne de la membrane cardiaque peut également être impliquée dans le processus. [ 2 ]
Des anomalies structurelles du myocarde (couche musculaire du cœur, constituée de cardiomyocytes), des mutations génétiques et des infections graves peuvent être à l'origine d'une forme courante de fibroélastose, lorsque non seulement l'endocarde, mais aussi le myocarde, sont impliqués. Généralement, des processus dysplasiques de l'endocarde, d'origines diverses, se produisent à la frontière de son contact avec la membrane musculaire, perturbant la contractilité de cette couche. Dans certains cas, on observe même une infiltration de la couche interne dans le myocarde, remplaçant les cardiomyocytes par des fibroblastes et des fibres, ce qui affecte la conduction de l'influx nerveux et le rythme cardiaque.
La compression des vaisseaux sanguins dans l'épaisseur de la membrane cardiaque par le myocarde épaissi perturbe la nutrition du myocarde (ischémie myocardique), ce qui peut à son tour entraîner une nécrose des tissus du muscle cardiaque.
La fibroélastose endocardique avec lésion du myocarde du cœur est appelée fibroélastose sous-endocardique ou endomyocardique.
Selon les statistiques, dans la plupart des cas de cette maladie rare (seulement 0,007 % du nombre total de nouveau-nés), une fibroélastose du ventricule gauche du cœur est diagnostiquée, bien que dans certains cas, le processus se propage également au ventricule droit et aux oreillettes, y compris les valves qui les séparent.
La fibroélastose cardiaque s'accompagne souvent de lésions des gros vaisseaux coronaires, également recouverts de tissu conjonctif. À l'âge adulte, elle survient souvent dans le contexte d'une athérosclérose vasculaire progressive.
La maladie est plus souvent observée dans les pays d’Afrique tropicale parmi les populations à faible niveau de vie, facilité par une mauvaise alimentation, des infections fréquentes et certains aliments et plantes consommés comme aliments.
Un épaississement endocardique est également observé au stade terminal de l'endocardite fibroplasique de Löffler, qui touche principalement les hommes d'âge moyen. La pathogénèse de cette maladie est également associée à des agents infectieux provoquant le développement d'une éosinophilie sévère, plus fréquente dans les infections parasitaires internes. Dans ce cas, les tissus de l'organisme (principalement le muscle cardiaque et le cerveau) commencent à souffrir d'un manque d'oxygène (hypoxie). Malgré la similitude des symptômes de la fibroélastose cardiaque et de l'endocardite fibreuse de Löffler, les médecins considèrent qu'il s'agit de maladies totalement différentes.
Causes fibroélastose
La fibroélastose désigne des modifications du tissu conjonctif des organes vitaux: le cœur et les poumons. Ces modifications s'accompagnent d'une perturbation du fonctionnement des organes et se reflètent sur l'apparence et l'état du patient. Les médecins connaissent cette maladie depuis des décennies. La fibroélastose de la paroi interne du cœur (endocarde) a été décrite dès le début du XVIIIe siècle, et des modifications similaires au niveau des poumons ont commencé à être évoquées deux siècles et demi plus tard. Cependant, les médecins ne sont pas encore parvenus à un accord définitif sur les causes de cette prolifération pathologique du tissu conjonctif.
Les causes exactes de la perturbation de la croissance et du développement des fibres conjonctives restent floues. Cependant, les scientifiques identifient certains facteurs de risque de ces changements, les considérant comme des causes possibles (mais non définitives) de la maladie.
Ainsi, dans la pathogenèse de la fibroélastose pulmonaire, considérée comme une maladie de l'âge mûr, un rôle particulier est attribué aux lésions infectieuses récurrentes de l'organe, observées chez la moitié des patients. Les infections provoquent une inflammation du tissu pulmonaire et de la plèvre, et une inflammation prolongée prédispose à leur transformation fibreuse.
Certains patients présentent des antécédents familiaux de fibroélastose, suggérant une prédisposition héréditaire. Des auto-anticorps non spécifiques ont été détectés dans leur organisme, provoquant des processus inflammatoires à long terme d'étiologie incertaine.
Certains pensent que des modifications fibreuses du tissu pulmonaire pourraient être causées par un reflux gastro-œsophagien. Ce lien est toutefois probablement indirect. On pense également que le risque de fibroélastose est plus élevé chez les personnes souffrant de maladies cardiovasculaires ou de thrombose pulmonaire.
La fibroélastose pulmonaire chez les jeunes et les adolescentes peut se manifester pendant la grossesse. Généralement, la maladie reste latente pendant une dizaine d'années ou plus, mais elle peut se manifester plus tôt, probablement en raison de la charge accrue de la femme enceinte et des changements hormonaux. Il n'existe pas encore d'explication précise. Néanmoins, une évolution similaire a été observée chez 30 % des patientes en âge de procréer examinées.
La grossesse elle-même ne peut pas provoquer la maladie, mais elle peut accélérer le développement des événements, ce qui est très triste, car le taux de mortalité de la maladie est très élevé et l'espérance de vie avec la fibroélastose est courte.
Dans la plupart des cas, la fibroélastose cardiaque est due à des maladies infantiles. Une pathologie congénitale est détectée en période prénatale chez un fœtus de 4 à 7 mois, mais le diagnostic ne peut être confirmé qu'après la naissance. Plusieurs facteurs peuvent être à l'origine de cette forme de la maladie: maladies infectieuses et inflammatoires transmises de la mère au fœtus, anomalies du développement des membranes cardiaques, insuffisance d'apport sanguin au tissu cardiaque, mutations génétiques et déficit en oxygène.
On pense que parmi les infections, les virus sont ceux qui contribuent le plus au développement de la fibroélastose cardiaque, car ils s'incrustent dans les cellules de l'organisme, les détruisent et modifient les propriétés des tissus. Le système immunitaire du fœtus, encore informe, ne peut le protéger contre ces agents pathogènes, contrairement à celui de la future mère. Cette dernière peut ne pas subir les conséquences d'une infection virale, tandis que chez le fœtus, une infection intra-utérine peut provoquer diverses anomalies.
Certains scientifiques pensent que le rôle déterminant dans la pathogenèse de la forme infectieuse de la fibroélastose est joué par une infection affectant le fœtus jusqu'à l'âge de 7 mois. Plus tard, elle peut uniquement provoquer des maladies inflammatoires du cœur (myocardite, endocardite).
Les anomalies dans le développement des membranes et des valves du cœur peuvent être provoquées à la fois par le processus inflammatoire et par des réactions auto-immunes inadéquates, à la suite desquelles les cellules du système immunitaire commencent à attaquer les propres cellules du corps.
Les mutations génétiques provoquent un développement anormal du tissu conjonctif, car les gènes contiennent des informations sur la structure et le comportement des structures protéiques (en particulier, les protéines de collagène et d'élastine).
L'hypoxie et l'ischémie du tissu cardiaque peuvent être la conséquence d'un développement cardiaque anormal. On parle alors de fibroélastose secondaire, provoquée par des malformations cardiaques congénitales (MCC). Celles-ci incluent des anomalies provoquant une obstruction (altération de la perméabilité du cœur et de ses vaisseaux):
- sténose ou rétrécissement de l'aorte près de la valve,
- coarctation ou rétrécissement segmentaire de l'aorte à la jonction de son arc et de sa section descendante,
- atrésie ou absence d'ouverture naturelle dans l'aorte,
- sous-développement du tissu cardiaque (le plus souvent le ventricule gauche, moins souvent le ventricule droit et les oreillettes), ce qui affecte la fonction de pompage du cœur.
Il existe une opinion selon laquelle la toxicose pendant la grossesse peut également agir comme un facteur prédisposant à la fibroélastose chez le fœtus.
En période postnatale, le développement de la fibroélastose cardiaque peut être favorisé par des maladies infectieuses et inflammatoires des membranes organiques, des troubles hémodynamiques consécutifs à des traumatismes, une thromboembolie vasculaire, une hémorragie myocardique, des troubles métaboliques (augmentation de la formation de fibrine, troubles du métabolisme des protéines et du fer: amylose, hémochromatose). Les mêmes causes sont à l'origine du développement de la maladie chez l'adulte.
Pathogénèse
Le tissu conjonctif est un tissu spécifique du corps humain, présent dans presque tous les organes, mais qui ne participe pas activement à leurs fonctions. On lui attribue des fonctions de soutien et de protection. Formant une sorte de squelette (structure, stroma) et limitant les cellules fonctionnelles de l'organe, il assure sa forme et sa taille définitives. Doté d'une résistance suffisante, le tissu conjonctif protège également les cellules de l'organe de la destruction et des blessures, prévient la pénétration d'agents pathogènes et, grâce à des macrophages spécifiques, absorbe les structures obsolètes: cellules mortes, protéines étrangères, déchets sanguins, etc.
Ce tissu peut être qualifié d'auxiliaire, car il ne contient pas les éléments cellulaires assurant la fonctionnalité de tel ou tel organe. Néanmoins, son rôle dans la vie de l'organisme est important. Constituant des membranes des vaisseaux sanguins, le tissu conjonctif assure la sécurité et la fonctionnalité de ces structures, permettant ainsi la nutrition et la respiration (trophisme) des tissus environnants.
Il existe plusieurs types de tissu conjonctif. La membrane qui recouvre les organes internes est appelée tissu conjonctif lâche. C'est une substance semi-liquide et incolore contenant des fibres de collagène ondulées et des fibres d'élastine droites, entre lesquelles sont dispersées de manière aléatoire différents types de cellules. Certaines de ces cellules (fibroblastes) sont responsables de la formation des structures fibreuses, d'autres (endothéliocytes et mastocytes) forment une matrice translucide de tissu conjonctif et produisent des substances spécifiques (héparine, histamine), d'autres encore (macrophages) assurent la phagocytose, etc.
Le deuxième type de tissu fibreux est le tissu conjonctif dense, peu riche en cellules individuelles. Il se divise en tissu blanc et tissu jaune. Le tissu blanc est constitué de fibres de collagène serrées (ligaments, tendons, périoste), tandis que le tissu jaune est constitué de fibres d'élastine entrelacées de manière chaotique, avec des inclusions de fibroblastes (partie des ligaments, des membranes des vaisseaux sanguins et des poumons).
Les tissus conjonctifs comprennent également le sang, la graisse, les os et le cartilage, mais nous ne nous y intéressons pas encore, car, lorsqu'on parle de fibroélastose, nous entendons des modifications des structures fibreuses. Or, les fibres élastiques et résilientes ne se trouvent que dans les tissus conjonctifs lâches et denses.
La synthèse des fibroblastes et la formation de fibres conjonctives à partir de ceux-ci sont régulées au niveau cérébral. Ceci assure la constance de ses caractéristiques (résistance, élasticité, épaisseur). Si, pour des raisons pathologiques, la synthèse et le développement du tissu auxiliaire sont perturbés (augmentation du nombre de fibroblastes, modification de leur comportement), on observe une prolifération de fibres de collagène résistantes ou une modification de la croissance des fibres élastiques (elles restent courtes, se tordent), ce qui entraîne une modification des propriétés de la membrane de l'organe et de certaines structures internes recouvertes de tissu conjonctif. Ces fibres acquièrent une épaisseur excessive, deviennent plus denses, plus résistantes et inélastiques, ressemblant au tissu fibreux des ligaments et des tendons, dont l'étirement nécessite un effort important.
Un tel tissu ne s'étire pas bien, limitant les mouvements de l'organe (mouvements rythmiques automatiques du cœur et des vaisseaux sanguins, changements de taille des poumons lors de l'inspiration et de l'expiration), d'où la perturbation de l'apport sanguin et des organes respiratoires, entraînant une carence en oxygène.
En fait, l'apport sanguin du corps est assuré par le cœur, qui fonctionne comme une pompe, et par deux circuits de circulation sanguine. La circulation pulmonaire est responsable de l'apport sanguin et des échanges gazeux dans les poumons, d'où l'oxygène est acheminé vers le cœur par le flux sanguin, puis vers la circulation systémique et distribué dans tout l'organisme, assurant la respiration des organes et des tissus.
La membrane élastique, limitant la contraction du muscle cardiaque, réduit la fonctionnalité du cœur, qui ne pompe plus aussi activement le sang, et donc l'oxygène. En cas de fibroélastose pulmonaire, la ventilation (osigénation) est altérée; il en résulte une diminution de l'apport d'oxygène dans le sang, ce qui, même avec une fonction cardiaque normale, contribue à une hypoxie des tissus et des organes. [ 3 ]
Symptômes fibroélastose
La fibroélastose cardiaque et la fibroélastose pulmonaire sont deux types de maladies caractérisées par un trouble de la synthèse des fibres du tissu conjonctif. Leur localisation est différente, mais elles peuvent toutes deux engager le pronostic vital, car elles sont associées à une insuffisance cardiaque et respiratoire progressive ou sévère.
La fibroélastose pulmonaire est une forme rare de maladie interstitielle de cet organe important du système respiratoire. Elle comprend des pathologies chroniques du parenchyme pulmonaire avec atteinte des parois alvéolaires (inflammation, altération de leur structure et de leur structure), de la paroi interne des capillaires pulmonaires, etc. La fibroélastose est souvent considérée comme une forme rare de pneumonie progressive, caractérisée par une tendance aux modifications fibreuses des tissus pulmonaires et pleuraux.
Il est quasiment impossible de détecter la maladie dès son apparition, car elle peut ne pas se manifester avant une dizaine d'années. Cette période est appelée « intervalle clair ». L'apparition de modifications pathologiques n'affectant pas encore le volume pulmonaire ni les échanges gazeux peut être détectée par hasard, lors d'un examen approfondi des poumons en lien avec une autre maladie ou blessure du système respiratoire.
La maladie se caractérise par une progression lente des symptômes, de sorte que les premières manifestations peuvent être considérablement retardées. Les symptômes s'intensifient progressivement.
Les premiers signes de la maladie à surveiller sont la toux et un essoufflement croissant. Ces symptômes sont souvent la conséquence d'une maladie respiratoire antérieure et peuvent donc être associés à un rhume et à ses conséquences à long terme. L'essoufflement est souvent perçu comme un trouble cardiaque ou des changements liés à l'âge. Après tout, la maladie est diagnostiquée chez les personnes approchant un âge avancé.
Des erreurs peuvent être commises par les patients et les médecins qui les examinent, ce qui conduit à une détection tardive d'une maladie dangereuse. Il convient de prêter attention à la toux, improductive en cas de fibroélastose, mais non stimulée par les mucolytiques et les expectorants, mais stoppée par les antitussifs. Une toux prolongée de ce type est un symptôme caractéristique de la fibroélastose pulmonaire.
La dyspnée est causée par une insuffisance respiratoire progressive due à un épaississement des parois alvéolaires et de la plèvre, ainsi qu'à une diminution du volume et du nombre de cavités alvéolaires dans le poumon (le parenchyme de l'organe est visible sur une radiographie comme un nid d'abeilles). Le symptôme s'intensifie sous l'effet d'un effort physique, d'abord important, puis même léger. À mesure que la maladie progresse, elle s'aggrave, entraînant une invalidité et le décès du patient.
La progression de la fibroélastose s'accompagne d'une détérioration de l'état général: l'hypoxie entraîne une faiblesse et des étourdissements, le poids corporel diminue (une anorexie se développe), les phalanges des ongles se transforment en type de pilons, la peau devient pâle et a un aspect maladif.
La moitié des patients développent des symptômes non spécifiques tels que des difficultés respiratoires et des douleurs thoraciques, caractéristiques d'un pneumothorax (accumulation de gaz dans la cavité pleurale). Cette anomalie peut également survenir à la suite de blessures, de maladies pulmonaires primaires ou secondaires, ou d'un traitement inapproprié, rendant son diagnostic impossible.
La fibroélastose cardiaque, ainsi que la pathologie de la croissance du tissu conjonctif dans les poumons, se caractérisent par: une pâleur de la peau, une perte de poids, une faiblesse souvent paroxystique et un essoufflement. Une température subfébrile persistante, sans signe de rhume ou d'infection, peut également être observée.
De nombreux patients constatent des modifications de la taille du foie. Ce dernier augmente de volume sans symptômes de dysfonctionnement. Un gonflement des jambes, du visage, des bras et de la région sacrée est également possible.
Une manifestation caractéristique de la maladie est une insuffisance circulatoire croissante associée à une perturbation cardiaque. Dans ce cas, on diagnostique une tachycardie (accélération du rythme cardiaque, souvent associée à une arythmie), un essoufflement (y compris en l'absence d'activité physique) et une cyanose tissulaire (coloration bleutée causée par l'accumulation de carboxyhémoglobine dans le sang, c'est-à-dire un composé d'hémoglobine et de dioxyde de carbone dû à une perturbation de la circulation sanguine et, par conséquent, des échanges gazeux).
Dans ce cas, les symptômes peuvent apparaître soit immédiatement après la naissance d'un enfant atteint de cette pathologie, soit sur une période plus longue. Chez les enfants plus âgés et les adultes, les signes d'insuffisance cardiaque sévère apparaissent généralement dans le contexte d'une infection respiratoire, qui agit comme déclencheur. [ 4 ]
Fibroélastose chez les enfants
Si la fibroélastose pulmonaire est une maladie de l'adulte, apparaissant souvent dès l'enfance, mais ne se manifestant pas avant longtemps, une pathologie similaire de l'endocarde cardiaque apparaît souvent avant même la naissance du bébé et affecte sa vie dès ses premiers instants. Cette pathologie rare mais grave est à l'origine du développement d'une insuffisance cardiaque difficile à corriger chez les nourrissons, dont beaucoup décèdent dans les deux ans. [ 5 ]
La fibroélastose endocardique du nouveau-né résulte dans la plupart des cas de processus pathologiques survenant dans l'organisme du bébé pendant la période prénatale. Infections transmises par la mère, mutations génétiques, anomalies du développement du système cardiovasculaire, maladies métaboliques héréditaires: selon les scientifiques, tout cela peut entraîner des modifications du tissu conjonctif des membranes cardiaques. Surtout si un fœtus de 4 à 7 mois est exposé simultanément à deux facteurs ou plus.
Par exemple, une combinaison d'anomalies du développement du cœur et des vaisseaux coronaires (sténose, atrésie, coarctation de l'aorte, développement anormal des cellules myocardiques, faiblesse endocardique, etc.), contribuant à l'ischémie tissulaire, combinée à un processus inflammatoire dû à une infection, laisse l'enfant avec pratiquement aucune chance de survie. Si les anomalies du développement des organes peuvent encore être corrigées rapidement, la fibroélastose progressive ne peut qu'être ralentie, mais non guérie.
Habituellement, la fibroélastose cardiaque fœtale est détectée dès la grossesse, lors d'une échographie au deuxième ou au troisième trimestre. L'échographie et l'échocardiographie réalisées entre 20 et 38 semaines ont révélé une hyperéchogénicité, témoignant d'un épaississement et d'une compaction de l'endocarde (généralement diffus, plus rarement focal), ainsi que d'une modification de la taille et de la forme du cœur (l'organe est élargi et prend la forme d'une boule ou d'une balle, et les structures internes sont progressivement lissées). [ 6 ]
Dans 30 à 35 % des cas, la fibroélastose a été détectée avant 26 semaines de grossesse, et dans 65 à 70 % des cas, au cours de la période suivante. Chez plus de 80 % des nouveau-nés, la fibroélastose est associée à une malformation cardiaque obstructive, c'est-à-dire secondaire, malgré sa détection précoce. Une hyperplasie ventriculaire gauche a été détectée chez la moitié des enfants atteints, ce qui explique la forte prévalence de la fibroélastose de cette structure cardiaque particulière. Les pathologies de l'aorte et de sa valve, diagnostiquées chez un tiers des enfants présentant une prolifération endocardique, entraînent également une dilatation de la cavité ventriculaire gauche et une altération de sa fonctionnalité.
En cas de fibroélastose cardiaque confirmée par un examen instrumental, les médecins recommandent l'interruption de grossesse. Chez la quasi-totalité des enfants nés de mères ayant refusé une interruption médicale de grossesse, les signes de la maladie ont été confirmés. Les symptômes d'insuffisance cardiaque, caractéristiques de la fibroélastose, apparaissent dans l'année qui suit (rarement entre la deuxième et la troisième année de vie). Chez les enfants atteints d'une forme combinée de la maladie, les signes d'insuffisance cardiaque sont détectés dès les premiers jours de vie.
Les formes congénitales de fibroélastose primaire et combinée chez l'enfant évoluent généralement rapidement et se transforment en insuffisance cardiaque sévère. Une faible activité, une léthargie, un refus d'allaiter dû à une fatigue rapide, un manque d'appétit et une transpiration excessive sont des signes de mauvaise santé. Tout cela conduit à une prise de poids difficile. La peau du bébé est douloureusement pâle, parfois bleutée, le plus souvent au niveau du triangle nasogénien.
Des signes d'immunité affaiblie apparaissent, ce qui rend ces enfants souvent et rapidement atteints d'infections respiratoires, ce qui complique la situation. Parfois, au cours des premiers jours et mois de vie, l'enfant ne présente aucun trouble circulatoire, mais des infections et des maladies pulmonaires fréquentes peuvent déclencher une insuffisance cardiaque congestive.
Des examens complémentaires chez les nouveau-nés et les jeunes enfants suspectés de fibroélastose ou ayant déjà reçu un diagnostic ont révélé une hypotension artérielle, une cardiomégalie, des sons étouffés à l'écoute du cœur, parfois un souffle systolique caractéristique d'une insuffisance mitrale, une tachycardie et une dyspnée. L'écoute pulmonaire révèle une respiration sifflante, signe d'une congestion.
Les lésions endocardiques du ventricule gauche entraînent souvent un affaiblissement de la couche musculaire du cœur (myocarde). Le rythme cardiaque normal est composé de deux sons alternant rythmiquement. En cas de fibroélastose, un troisième (et parfois un quatrième) son peut apparaître. Ce rythme pathologique est clairement audible et ressemble à la démarche à trois temps d'un cheval (galop), d'où son nom de rythme de galop.
Un autre symptôme de la fibroélastose chez le jeune enfant est l'apparition d'une bosse cardiaque. En effet, les côtes de l'enfant, au début de la période postnatale, restent non ossifiées et sont constituées de tissu cartilagineux. L'augmentation de la taille du cœur entraîne une pression sur les côtes « molles », qui se courbent et prennent une forme définitivement incurvée vers l'avant (bosse cardiaque). Chez l'adulte, la fibroélastose empêche la formation de bosse cardiaque grâce à la résistance et à la rigidité du tissu osseux des côtes, même en cas d'augmentation de toutes les structures cardiaques.
La formation d'une bosse cardiaque n'indique en elle-même qu'une malformation cardiaque congénitale, sans en préciser la nature. Dans tous les cas, elle est associée à une augmentation de la taille du cœur et de ses ventricules.
Le syndrome d'œdème dans la fibroélastose chez les enfants est rarement diagnostiqué, mais de nombreux enfants présentent une hypertrophie du foie, qui commence à dépasser en moyenne de 3 cm sous le bord de l'arc costal.
Si la fibroélastose est acquise (par exemple, suite à une maladie inflammatoire des membranes cardiaques), le tableau clinique est le plus souvent d'évolution lente. Pendant un certain temps, les symptômes peuvent être totalement absents, puis des signes légers de dysfonctionnement cardiaque apparaissent: essoufflement à l'effort, accélération du rythme cardiaque, fatigue rapide et faible endurance physique. Un peu plus tard, le foie commence à grossir, des œdèmes et des vertiges apparaissent.
Tous les symptômes de la fibroélastose acquise sont non spécifiques, ce qui complique le diagnostic de la maladie, qui évoque une cardiomyopathie, une maladie hépatique ou rénale. La maladie est le plus souvent diagnostiquée au stade d'insuffisance cardiaque sévère, ce qui affecte négativement les résultats du traitement.
Complications et conséquences
Il convient de préciser que la fibroélastose cardiaque et pulmonaire est une pathologie grave, dont l'évolution dépend de diverses circonstances. Les malformations cardiaques congénitales compliquent considérablement la situation, et peuvent être traitées chirurgicalement à un âge précoce. Cependant, le risque de décès demeure assez élevé (environ 10 %).
On pense que plus la maladie se développe tôt, plus ses conséquences seront graves. Ceci est confirmé par le fait que la fibroélastose congénitale évolue dans la plupart des cas de manière fulminante ou aiguë, avec une progression rapide de l'insuffisance cardiaque. Le développement d'une insuffisance cardiaque aiguë chez un enfant de moins de 6 mois est considéré comme un signe de mauvais pronostic.
Cependant, le traitement ne garantit pas le rétablissement complet de la fonction cardiaque, mais ralentit seulement la progression des symptômes de l'insuffisance cardiaque. En revanche, l'absence de traitement de soutien peut entraîner le décès du bébé dans les deux premières années de vie.
Si une insuffisance cardiaque est détectée dans les premiers jours ou mois de la vie d'un bébé, il est fort probable que l'enfant ne survive pas plus d'une semaine. La réponse au traitement varie selon les enfants. En l'absence d'effet thérapeutique, il n'y a pratiquement aucun espoir. Cependant, avec l'aide apportée, l'espérance de vie d'un enfant malade est courte (de quelques mois à plusieurs années).
La chirurgie et la correction des malformations cardiaques congénitales à l'origine de la fibroélastose améliorent généralement l'état du patient. Avec un traitement chirurgical réussi de l'hyperplasie ventriculaire gauche et le respect des prescriptions médicales, la maladie peut évoluer vers une évolution bénigne: l'insuffisance cardiaque évoluera vers une évolution chronique sans signe de progression. Cependant, l'espoir d'un tel résultat est faible.
Quant à la forme acquise de fibroélastose cardiaque, elle devient rapidement chronique et progresse progressivement. Les médicaments peuvent ralentir le processus, mais pas l'arrêter.
La fibroélastose pulmonaire, quel que soit le moment d'apparition des modifications du parenchyme et des membranes de l'organe après la période de lumière, progresse rapidement et peut entraîner le décès en quelques années, provoquant une insuffisance respiratoire sévère. Malheureusement, aucun traitement efficace n'a encore été développé. [ 7 ]
Diagnostics fibroélastose
La fibroélastose endomyocardique, dont les symptômes sont généralement détectés à un âge précoce, est une maladie congénitale. Si l'on exclut les rares cas où la maladie s'est développée à la fin de l'enfance et à l'âge adulte, suite à une complication de blessures et de maladies somatiques, il est possible d'identifier la pathologie dès la période prénatale, c'est-à-dire avant la naissance de l'enfant.
Les médecins estiment que les modifications pathologiques des tissus endocardiques, les modifications de la forme du cœur fœtal et certaines caractéristiques de son fonctionnement, caractéristiques de la fibroélastose, peuvent être détectées dès la 14e semaine de grossesse. Cependant, cette période reste relativement courte, et il n'est pas exclu que la maladie se manifeste un peu plus tard, vers le troisième trimestre de grossesse, et parfois quelques mois avant l'accouchement. C'est pourquoi, lors du suivi des femmes enceintes, il est recommandé de réaliser des échographies cardiaques fœtales à intervalles de plusieurs semaines.
Quels signes permettent aux médecins de suspecter la maladie lors de l'échographie suivante? Tout dépend de la forme de la maladie. Le plus souvent, la fibroélastose est diagnostiquée au niveau du ventricule gauche, mais cette structure n'est pas toujours élargie. La forme dilatée de la maladie avec un ventricule gauche élargi est facilement identifiée lors d'une échographie par la forme sphérique du cœur, dont l'apex est représenté par le ventricule gauche, l'augmentation générale de la taille de l'organe et le renflement du septum interventriculaire vers le ventricule droit. Cependant, le principal signe de fibroélastose est l'épaississement de l'endocarde et des septa cardiaques, avec une augmentation caractéristique de l'échogénicité de ces structures, ce qui est mis en évidence par une échographie spécifique.
L'examen est réalisé à l'aide d'un équipement d'échographie spécifique et de programmes de cardiologie. L'échocardiographie fœtale est sans danger pour la mère et l'enfant à naître, et permet non seulement d'identifier les modifications anatomiques du cœur, mais aussi de déterminer l'état des vaisseaux coronaires, la présence de caillots sanguins et les modifications de l'épaisseur des membranes cardiaques.
L'échocardiographie fœtale est prescrite non seulement en présence d'écarts lors du décodage des résultats de l'échographie, mais également en cas d'infection de la mère (notamment virale), de prise de médicaments puissants, de prédisposition héréditaire, de présence de troubles métaboliques, ainsi que de pathologies cardiaques congénitales chez les enfants plus âgés.
L'échocardiographie fœtale permet également de détecter d'autres formes congénitales de fibroélastose. Par exemple, la fibroélastose du ventricule droit, un processus étendu avec atteinte simultanée du ventricule gauche et des structures adjacentes: ventricule droit, valves cardiaques, oreillettes, formes combinées de fibroélastose, fibroélastose endomyocardique avec épaississement de la paroi interne des ventricules et atteinte d'une partie du myocarde dans le processus pathologique (généralement associée à une thrombose de la paroi).
La fibroélastose endocardique détectée avant la naissance a un pronostic très sombre; les médecins recommandent donc l'interruption de grossesse dans ce cas. La possibilité d'un diagnostic erroné est exclue par une nouvelle échographie du cœur fœtal, réalisée quatre semaines après le premier examen ayant révélé la pathologie. Il est clair que la décision finale d'interrompre ou de poursuivre la grossesse appartient aux parents, mais ils doivent être conscients du mode de vie auquel ils condamnent l'enfant.
La fibroélastose endocardique n'est pas toujours détectée pendant la grossesse, d'autant plus que toutes les femmes enceintes ne s'inscrivent pas dans une clinique de santé féminine et ne subissent pas d'échographie préventive. La présence d'un enfant malade dans l'utérus n'a pratiquement aucun effet sur l'état de la femme enceinte; la naissance d'un bébé malade est donc souvent une mauvaise surprise.
Dans certains cas, les parents et les médecins découvrent la maladie du bébé plusieurs mois après sa naissance. Dans ce cas, les analyses sanguines peuvent ne rien révéler, si ce n'est une augmentation de la concentration de sodium (hypernatrémie). Leurs résultats seront toutefois utiles pour réaliser un diagnostic différentiel et exclure une maladie inflammatoire.
Il existe encore de l'espoir pour le diagnostic instrumental. Un examen cardiaque standard (ECG) n'est pas particulièrement révélateur en cas de fibroélastose. Il permet d'identifier des troubles cardiaques et de la conductivité électrique du muscle cardiaque, mais n'en précise pas les causes. Ainsi, une variation de la tension ECG (généralement sous-estimée à un jeune âge, et excessivement élevée à un âge avancé) indique une cardiomyopathie, qui peut être associée non seulement à des pathologies cardiaques, mais aussi à des troubles métaboliques. La tachycardie est un symptôme de maladies cardiaques. Si les deux ventricules du cœur sont touchés, le cardiogramme peut généralement paraître normal. [ 8 ]
La tomodensitométrie (TDM) est un excellent outil non invasif pour détecter la calcification cardiovasculaire et exclure la péricardite.[ 9 ]
L'imagerie par résonance magnétique (IRM) peut être utile pour détecter la fibroélastose, car la biopsie est invasive. Un bord hypointense sur une séquence de perfusion myocardique et un bord hyperintense sur une séquence de rehaussement retardé suggèrent une fibroélastose.[ 10 ]
Mais cela ne signifie pas que l’étude doit être abandonnée, car elle permet de déterminer la nature du travail du cœur et le degré de développement de l’insuffisance cardiaque.
Lorsque des symptômes d'insuffisance cardiaque apparaissent et que le patient consulte un médecin, on lui prescrit également une radiographie pulmonaire, une tomodensitométrie ou une imagerie par résonance magnétique (IRM) du cœur, ainsi qu'une échocardiographie (EchoCG). En cas de doute, il est nécessaire de recourir à une biopsie du tissu cardiaque suivie d'un examen histologique. Le diagnostic est très grave et nécessite donc la même approche diagnostique, bien que le traitement ne diffère guère du traitement symptomatique de la maladie coronarienne et de l'insuffisance cardiaque.
Mais même un examen aussi scrupuleux ne sera d'aucune utilité si ses résultats ne sont pas utilisés dans le diagnostic différentiel. L'ECG permet de différencier une fibroélastose aiguë d'une myocardite idiopathique, d'une péricardite exsudative ou d'une sténose aortique. Parallèlement, les analyses de laboratoire ne montreront pas de signes d'inflammation (leucocytose, augmentation de la VS, etc.) et les mesures de température ne montreront pas d'hyperthermie.
L'analyse des bruits et des souffles cardiaques, les modifications de la taille des oreillettes et l'étude de l'anamnèse aident à distinguer la fibroélastose endocardique de l'insuffisance mitrale isolée et du défaut de la valve mitrale.
L'analyse des données anamnestiques permet de distinguer la fibroélastose d'une sténose cardiaque ou aortique. En cas de sténose aortique, il convient également de veiller au maintien du rythme sinusal et à l'absence de thromboembolie. La péricardite exsudative ne présente pas non plus de troubles du rythme cardiaque ni de dépôt de thrombus, mais la maladie se manifeste par une augmentation de la température et de la fièvre.
La plus grande difficulté réside dans la distinction entre fibroélastose endocardique et cardiomyopathie congestive. Dans ce cas, la fibroélastose, bien que généralement non accompagnée de troubles prononcés de la conduction cardiaque, a un pronostic thérapeutique moins favorable.
En cas de pathologies combinées, il est nécessaire de prêter attention à toute anomalie révélée lors d'une tomographie ou d'une échographie cardiaque, car les anomalies congénitales compliquent considérablement l'évolution de la fibroélastose. Si une fibroélastose endocardique combinée est détectée pendant la période intra-utérine, il est inapproprié de poursuivre la grossesse. Il est beaucoup plus humain d'y mettre fin.
Diagnostic de la fibroélastose pulmonaire
Le diagnostic de la fibroélastose pulmonaire requiert également certaines connaissances et compétences de la part du médecin. En effet, les symptômes de la maladie sont très hétérogènes. D'une part, ils peuvent indiquer une pneumopathie congestive (toux non productive, essoufflement) et, d'autre part, ils peuvent également être la manifestation d'une pathologie cardiaque. Par conséquent, le diagnostic de la maladie ne peut se résumer à la simple constatation des symptômes et à l'auscultation.
Les analyses sanguines du patient permettent d'exclure une pneumopathie inflammatoire, mais ne renseignent pas sur les modifications quantitatives et qualitatives des tissus. La présence de signes d'éosinophilie permet de différencier la maladie d'une fibrose pulmonaire, dont les manifestations sont similaires, mais ne permet pas d'infirmer ni de confirmer la présence d'une fibroélastose.
Les études instrumentales sont considérées comme plus indicatives: radiographie thoracique et examen tomographique des organes respiratoires, ainsi que les analyses fonctionnelles, qui consistent à déterminer les volumes respiratoires, la capacité vitale des poumons et la pression dans l'organe.
En cas de fibroélastose pulmonaire, il convient de prêter attention à la diminution de la fonction respiratoire externe, mesurée par spirométrie. La diminution des cavités alvéolaires actives affecte significativement la capacité vitale des poumons (VCL), et l'épaississement des parois des structures internes affecte la capacité de diffusion de l'organe (DCL), qui assure les fonctions de ventilation et d'échange gazeux (en termes simples, l'absorption du dioxyde de carbone du sang et la libération d'oxygène).
Les signes caractéristiques de la fibroélastose pleuroparenchymateuse sont une combinaison d'un flux d'air limité dans les poumons (obstruction) et d'une expansion pulmonaire altérée lors de l'inhalation (restriction), une détérioration de la fonction respiratoire externe, une hypertension pulmonaire modérée (augmentation de la pression dans les poumons), diagnostiquée chez la moitié des patients.
Une biopsie pulmonaire révèle des modifications caractéristiques de la structure interne de l'organe. Parmi celles-ci: une fibrose de la plèvre et du parenchyme associée à une élastose des parois alvéolaires, une accumulation de lymphocytes au niveau des cloisons alvéolaires compactées, une transformation atypique des fibroblastes en tissu musculaire et la présence de liquide œdémateux.
La tomographie montre des lésions pulmonaires dans les parties supérieures, sous forme de foyers de compaction pleurale et de modifications structurelles du parenchyme. Le tissu conjonctif pulmonaire hypertrophié ressemble au tissu musculaire par sa couleur et ses propriétés, mais son volume diminue. Des cavités aérées (kystes) assez importantes sont présentes dans le parenchyme. Une dilatation focale (ou diffuse) irréversible des bronches et des bronchioles (bronchectasie de traction) et une position basse du dôme diaphragmatique sont caractéristiques.
Les examens radiologiques révèlent des zones de « verre dépoli » et de « poumon en nid d'abeille » chez de nombreux patients, indiquant une ventilation pulmonaire inégale due à la présence de foyers de compaction tissulaire. Environ la moitié des patients présentent une hypertrophie des ganglions lymphatiques et du foie.
La fibroélastose pulmonaire doit être différenciée de la fibrose causée par une infection parasitaire et une éosinophilie associée, de la fibroélastose endocardique, des maladies pulmonaires avec ventilation altérée et image de « poumon en nid d'abeille », de la maladie auto-immune histicotite X (une forme de cette pathologie avec atteinte pulmonaire est appelée maladie de Hand-Schüller-Christian), des manifestations de la sarcoïdose et de la tuberculose pulmonaire.
Traitement fibroélastose
La fibroélastose, quelle que soit sa localisation, est considérée comme une maladie dangereuse et pratiquement incurable. Les modifications pathologiques de la plèvre et du parenchyme pulmonaire ne peuvent être corrigées par des médicaments. Même l'utilisation d'anti-inflammatoires hormonaux (corticoïdes) en association avec des bronchodilatateurs ne donne pas le résultat escompté. Les bronchodilatateurs contribuent à soulager légèrement l'état du patient, soulageant le syndrome obstructif, mais n'ayant aucun effet sur les processus pulmonaires, ils ne peuvent être utilisés qu'en traitement de soutien.
Le traitement chirurgical de la fibroélastose pulmonaire est également inefficace. La seule intervention susceptible de changer la situation est la transplantation d'organe. Mais la transplantation pulmonaire, hélas, présente le même pronostic défavorable. [ 11 ]
Selon des scientifiques étrangers, la fibroélastose peut également être considérée comme l'une des complications fréquentes de la transplantation de cellules souches pulmonaires ou de moelle osseuse. Dans les deux cas, des modifications se produisent dans les fibres du tissu conjonctif pulmonaire, affectant la fonction respiratoire externe.
La maladie progresse sans traitement (et il n'existe actuellement aucun traitement efficace), et environ 40 % des patients décèdent d'insuffisance respiratoire dans un délai de 1,5 à 2 ans. L'espérance de vie des personnes survivantes est également fortement limitée (jusqu'à 10 à 20 ans), tout comme leur capacité à travailler. La personne devient invalide.
La fibroélastose cardiaque est également considérée comme une maladie médicalement incurable, surtout s'il s'agit d'une pathologie congénitale. En général, les enfants ne vivent pas plus de deux ans. Seule une transplantation cardiaque peut les sauver, opération complexe et à haut risque, aux conséquences imprévisibles, surtout à un si jeune âge.
Chez certains bébés, il est possible de corriger chirurgicalement les malformations cardiaques congénitales afin de ne pas aggraver leur état. En cas de sténose artérielle, un dilatateur vasculaire (shunt) est installé (pontage aortocoronarien). En cas de dilatation du ventricule gauche, sa forme est rapidement rétablie. Cependant, même une telle opération ne garantit pas que l'enfant puisse se passer d'une greffe. Environ 20 à 25 % des bébés survivent et souffrent d'insuffisance cardiaque toute leur vie; ils ne sont donc pas considérés comme en bonne santé.
Si la maladie est contractée, il est important de lutter pour la survie de l'enfant grâce à des médicaments. Mais il est important de comprendre que plus la maladie se manifeste tôt, plus il sera difficile de la combattre.
Le traitement médicamenteux vise à prévenir et à combattre les exacerbations de l'insuffisance cardiaque. Les patients se voient prescrire les médicaments cardiaques suivants:
- les inhibiteurs de l'enzyme de conversion de l'angiotensine (ECA), qui agissent sur la pression artérielle et la maintiennent dans les limites normales (captopril, énalapril, bénazépril, etc.),
- bêtabloquants utilisés pour traiter les troubles du rythme cardiaque, l'hypertension artérielle et prévenir l'infarctus du myocarde (anapriline, bisoprolol, métoprolol),
- glycosides cardiaques qui, lorsqu'ils sont utilisés sur une longue période, non seulement soutiennent le fonctionnement du cœur (augmentent la teneur en potassium des cardiomyocytes et améliorent la conductivité myocardique), mais sont également capables de réduire quelque peu le degré d'épaississement endocardique (digoxine, gitoxine, strophanthine),
- diurétiques épargneurs de potassium (spironolactone, véroshpiron, decriz), prévenant l'œdème tissulaire,
- traitement antithrombotique avec des anticoagulants (cardiomagnyl, magnicor), prévenant la formation de caillots sanguins et les troubles circulatoires dans les vaisseaux coronaires.
Dans la forme congénitale de la fibroélastose endocardique, le traitement de soutien ne favorise pas la guérison, mais réduit le risque de décès par insuffisance cardiaque ou thromboembolie de 70 à 75 %. [ 12 ]
Médicaments
Comme on peut le constater, le traitement de la fibroélastose endocardique est pratiquement identique à celui de l'insuffisance cardiaque. Dans les deux cas, les cardiologues prennent en compte la gravité de la cardiopathie. La prescription des médicaments est strictement individuelle, tenant compte de l'âge du patient, des maladies concomitantes, de la forme et du degré de l'insuffisance cardiaque.
Dans le traitement de la fibroélastose endocardique acquise, des médicaments de cinq groupes sont utilisés. Examinons un médicament de chaque groupe.
L'énalapril est un médicament du groupe des inhibiteurs de l'ECA, disponible sous forme de comprimés à différents dosages. Il augmente le flux sanguin coronaire, dilate les artères, réduit la tension artérielle sans affecter la circulation cérébrale, ralentit et réduit la dilatation du ventricule gauche. Il améliore l'apport sanguin au myocarde, réduisant ainsi les effets de l'ischémie, réduit légèrement la coagulation sanguine et prévient la formation de caillots sanguins, et possède un léger effet diurétique.
En cas d'insuffisance cardiaque, le médicament est prescrit pour une durée supérieure à six mois ou à titre permanent. Le traitement est débuté à la dose minimale (2,5 mg), puis augmenté progressivement de 2,5 à 5 mg tous les 3 à 4 jours. La dose permanente sera celle bien tolérée par le patient et maintiendra la tension artérielle dans les limites de la normale.
La dose quotidienne maximale est de 40 mg. Elle peut être prise en une seule prise ou divisée en deux prises.
Si la tension artérielle est inférieure à la normale, la dose est progressivement réduite. Le traitement par énalapril ne doit pas être interrompu brutalement. Il est recommandé de prendre une dose d'entretien de 5 mg par jour.
Ce médicament est destiné au traitement des patients adultes, mais peut également être prescrit aux enfants (son innocuité n'a pas été officiellement établie, mais en cas de fibroélastose, la vie d'un jeune patient est en jeu; le rapport risque/risque est donc pris en compte). L'inhibiteur de l'ECA n'est pas prescrit aux patients présentant une intolérance aux composants du médicament, à la porphyrie, à la grossesse et à l'allaitement. Si le patient a déjà présenté un œdème de Quincke lors de la prise de médicaments de ce groupe, l'énalapril est interdit.
La prudence est de mise lors de la prescription du médicament à des patients présentant des pathologies concomitantes: maladies rénales et hépatiques graves, hyperkaliémie, hyperaldostéronisme, sténose de la valve aortique ou mitrale, pathologies systémiques du tissu conjonctif, ischémie cardiaque, maladie cérébrale, diabète sucré.
Lors du traitement par ce médicament, il est déconseillé de prendre des diurétiques conventionnels afin d'éviter une déshydratation et un fort effet hypotenseur. L'administration concomitante de diurétiques épargneurs de potassium nécessite un ajustement posologique, car le risque d'hyperkaliémie est élevé, ce qui peut provoquer des arythmies cardiaques, des convulsions, une diminution du tonus musculaire, une faiblesse accrue, etc.
L'énalapril est généralement bien toléré, mais certains patients peuvent présenter des effets secondaires. Les plus fréquents sont: une forte baisse de la tension artérielle pouvant aller jusqu'au collapsus, des maux de tête et des étourdissements, des troubles du sommeil, une fatigue accrue, une perte réversible de l'équilibre, de l'ouïe et de la vue, l'apparition d'acouphènes, un essoufflement, une toux sans expectorations, des modifications de la composition du sang et des urines, généralement révélatrices d'un dysfonctionnement hépatique et rénal. Parmi les effets secondaires possibles: perte de cheveux, baisse de la libido, bouffées de chaleur (sensation de chaleur et palpitations, rougeur de la peau du visage, etc.).
Le bisoprolol est un bêtabloquant à action sélective, doté d'effets hypotenseurs et anti-ischémiques, qui aide à lutter contre les manifestations de tachycardie et d'arythmie. Il s'agit d'un médicament économique sous forme de comprimés, qui prévient la progression de l'insuffisance cardiaque dans la fibroélastose endocardique. [ 13 ]
Comme de nombreux autres médicaments prescrits pour les maladies coronariennes et l'ICC, le bisoprolol est prescrit sur une longue durée. Il est conseillé de le prendre le matin, avant ou pendant les repas.
Les dosages recommandés sont choisis individuellement en fonction de la tension artérielle et des médicaments prescrits en parallèle. En moyenne, une dose unique (y compris quotidienne) est de 5 à 10 mg, mais en cas de légère augmentation de la tension, elle peut être réduite à 2,5 mg. La dose maximale prescrite à un patient dont les reins fonctionnent normalement est de 20 mg, mais uniquement en cas d'hypertension artérielle persistante.
L'augmentation des doses indiquées n'est possible qu'avec l'autorisation d'un médecin. Cependant, en cas de maladies hépatiques et rénales graves, la dose maximale autorisée est de 10 mg.
Dans le traitement complexe de l'insuffisance cardiaque sur fond de dysfonction ventriculaire gauche, le plus souvent associée à la fibroélastose, la dose efficace est choisie en augmentant progressivement la dose de 1,25 mg. Dans ce cas, la dose minimale (1,25 mg) est initialement administrée. La dose est augmentée toutes les semaines.
Lorsque la dose atteint 5 mg, l'intervalle est porté à 28 jours. Après 4 semaines, la dose est augmentée de 2,5 mg. En respectant cet intervalle et cette norme, la dose atteint 10 mg, que le patient devra prendre pendant une longue période ou de manière continue.
Si une telle posologie est mal tolérée, elle est progressivement réduite jusqu'à un niveau confortable. L'arrêt du traitement par bêtabloquant ne doit pas non plus être brutal.
Le médicament ne doit pas être prescrit en cas d'hypersensibilité aux substances actives et auxiliaires du médicament, d'insuffisance cardiaque aiguë et décompensée, de choc cardiogénique, de bloc auriculo-ventriculaire de grade 2-3, de bradycardie, d'hypotension artérielle constante et de certaines autres pathologies cardiaques, d'asthme bronchique sévère, de broncho-obstruction, de troubles circulatoires périphériques sévères, d'acidose métabolique.
La prudence est de mise lors de la prescription d'un traitement complexe. Ainsi, l'association du bisoprolol avec certains antiarythmiques (quinidine, lidocaïne, phénytoïne, etc.), les antagonistes calciques et les hypotenseurs centraux est déconseillée.
Symptômes et troubles désagréables possibles pendant le traitement par bisoprolol: fatigue accrue, maux de tête, bouffées de chaleur, troubles du sommeil, chute de tension artérielle et vertiges au lever, perte auditive, symptômes gastro-intestinaux, troubles hépatiques et rénaux, diminution de l'activité sexuelle, faiblesse musculaire et crampes. Les patients se plaignent parfois de troubles circulatoires périphériques, se manifestant par une baisse de température ou un engourdissement des extrémités, en particulier des doigts et des orteils.
En présence de maladies concomitantes du système bronchopulmonaire, des reins, du foie et du diabète sucré, le risque d'effets indésirables est plus élevé, ce qui indique une exacerbation de la maladie.
La digoxine est un glycoside cardiaque populaire et économique, issu de la digitale. Délivré strictement sur ordonnance (sous forme de comprimés), il doit être utilisé sous la surveillance d'un professionnel de santé. Le traitement par injection est réalisé en milieu hospitalier lors d'une exacerbation de maladie coronarienne et d'insuffisance cardiaque congestive. Les comprimés sont prescrits de manière continue à des doses minimales, car le médicament a un effet toxique et narcotique.
L'effet thérapeutique consiste à modifier l'intensité et l'amplitude des contractions myocardiques (apport d'énergie au cœur et soutien en cas d'ischémie). Le médicament possède également un effet vasodilatateur (décongestionnant) et diurétique, contribuant à soulager l'œdème et à réduire la gravité de l'insuffisance respiratoire, se manifestant par un essoufflement.
Le danger de la digoxine et des autres glycosides cardiaques est qu’en cas de surdosage, ils peuvent provoquer une arythmie cardiaque causée par une excitabilité accrue du myocarde.
En cas d'exacerbation de l'ICC, le médicament est prescrit sous forme d'injections, la posologie étant adaptée à la gravité de l'affection et à l'âge du patient. Une fois l'état stabilisé, le traitement passe aux comprimés.
Habituellement, la dose unique standard du médicament est de 0,25 mg. La fréquence d'administration peut varier de 1 à 5 fois par jour, à intervalles réguliers. Au stade aigu de l'ICC, la dose quotidienne peut atteindre 1,25 mg. Lorsque l'état se stabilise durablement, il est nécessaire de prendre une dose d'entretien de 0,25 mg (plus rarement 0,5 mg) par jour.
Lors de la prescription du médicament aux enfants, le poids du patient est pris en compte. Une dose efficace et sûre est calculée entre 0,05 et 0,08 mg par kg de poids corporel. Cependant, le médicament n'est pas prescrit en continu, mais pendant 1 à 7 jours.
La posologie des glycosides cardiaques doit être prescrite par un médecin, en tenant compte de l'état et de l'âge du patient. Cependant, il est très dangereux d'ajuster les doses indépendamment ou de prendre simultanément deux médicaments ayant un tel effet.
La digoxine n'est pas prescrite en cas d'angor instable, d'arythmies cardiaques sévères, de bloc auriculo-ventriculaire de grade 2-3, de tamponnade cardiaque, de syndrome d'Adams-Stokes-Morgagni, de sténose bicuspide isolée et de sténose aortique, d'anomalie cardiaque congénitale appelée syndrome de Wolff-Parkinson-White, de cardiomyopathie hypertrophique obstructive, d'endocardite, de péricardite et de myocardite, d'anévrisme de l'aorte thoracique, d'hypercalcémie, d'hypokaliémie et de certaines autres pathologies. La liste des contre-indications est assez longue et comprend des syndromes aux manifestations multiples; la décision d'utiliser ce médicament ne peut donc être prise que par un spécialiste.
La digoxine présente également des effets secondaires. Parmi ceux-ci figurent des troubles du rythme cardiaque (consécutifs à une dose mal choisie ou à un surdosage), une perte d'appétit, des nausées (souvent accompagnées de vomissements), des troubles intestinaux, une faiblesse et une fatigue intenses, des maux de tête, des rougeurs, une diminution du taux de plaquettes et des troubles de la coagulation sanguine, ainsi que des réactions allergiques. Le plus souvent, l'apparition de ces symptômes et d'autres est associée à la prise de fortes doses du médicament, plus rarement à un traitement prolongé.
La spironolactone est un antagoniste des minéralocorticoïdes. Elle a un effet diurétique, favorisant l'excrétion du sodium, du chlore et de l'eau, tout en préservant le potassium, indispensable au fonctionnement normal du cœur, dont la fonction conductrice repose principalement sur cet élément. Elle contribue à soulager les œdèmes. Elle est utilisée comme adjuvant dans l'insuffisance cardiaque congestive.
En cas d'ICC, le médicament est prescrit en fonction du stade de la maladie. En cas d'exacerbation, le médicament peut être prescrit sous forme d'injections ou de comprimés, à une dose de 50 à 100 mg par jour. Une fois l'état stabilisé, une dose d'entretien de 25 à 50 mg est prescrite pendant une longue période. Si l'équilibre potassium-sodium est perturbé et conduit à une diminution du potassium-sodium, la dose peut être augmentée jusqu'à ce qu'une concentration normale en oligo-éléments soit rétablie.
En pédiatrie, la dose efficace est calculée sur la base d'un rapport de 1 à 3 mg de spironolactone par kilogramme de poids corporel du patient.
Comme on peut le constater, ici aussi, le choix de la dose recommandée est individuel, comme c'est le cas pour la prescription de nombreux autres médicaments utilisés en cardiologie.
Les contre-indications à l'utilisation d'un diurétique peuvent être: un excès de potassium ou un faible taux de sodium, une pathologie associée à l'absence de miction (anurie), une maladie rénale sévère avec altération des performances. Ce médicament est déconseillé aux femmes enceintes et allaitantes, ainsi qu'aux personnes présentant une intolérance à ses composants.
La prudence est de mise lors de l'utilisation du médicament chez les patients présentant un bloc auriculo-ventriculaire (pouvant s'aggraver), un excès de calcium (hypercalcémie), une acidose métabolique, un diabète sucré, des irrégularités menstruelles et une maladie du foie.
La prise de ce médicament peut provoquer des maux de tête, une somnolence, une perte d'équilibre et de coordination des mouvements (ataxie), une augmentation du volume des glandes mammaires chez l'homme (gynécomastie) et une impuissance, des modifications du cycle menstruel, une voix rauque et une pilosité excessive chez la femme (hirsutisme), des douleurs épigastriques et des troubles gastro-intestinaux, des coliques intestinales, un dysfonctionnement rénal et un déséquilibre minéral. Des réactions cutanées et allergiques sont possibles.
Des effets secondaires sont généralement observés lorsque la dose requise est dépassée. Un œdème peut survenir lorsque la dose est insuffisante.
« Magnicor » est un médicament anti-thrombotique à base d'acide acétylsalicylique et d'hydroxyde de magnésium. Il est l'un des traitements antithrombotiques les plus efficaces prescrits en cas d'insuffisance cardiaque. Il possède des propriétés analgésiques, anti-inflammatoires et antiplaquettaires, et affecte la fonction respiratoire. L'hydroxyde de magnésium réduit l'effet négatif de l'acide acétylsalicylique sur la muqueuse gastro-intestinale.
En cas de fibroélastose endomyocardique, le médicament est prescrit à titre prophylactique. La dose minimale efficace est donc de 75 mg, soit 1 comprimé. En cas d'ischémie cardiaque due à la formation d'un thrombus et au rétrécissement ultérieur de la lumière des vaisseaux coronaires, la dose initiale est de 2 comprimés, et la dose d'entretien correspond à la dose prophylactique.
Dépasser la dose recommandée augmente considérablement le risque de saignement difficile à arrêter.
Les dosages sont indiqués pour les patients adultes en raison du fait que le médicament contient de l'acide acétylsalicylique, dont l'utilisation à l'âge de moins de 15 ans peut avoir de graves conséquences.
Le médicament n'est pas prescrit aux patients de l'enfance et du début de l'adolescence, en cas d'intolérance à l'acide acétylsalicylique et aux autres composants du médicament, d'asthme à l'aspirine (dans les antécédents), de gastrite érosive aiguë, d'ulcère gastroduodénal, de diathèse hémorragique, de maladies graves du foie et des reins, en cas d'insuffisance cardiaque décompensée sévère.
Pendant la grossesse, Magnicor n'est prescrit qu'en cas d'extrême nécessité et uniquement au cours du premier ou du deuxième trimestre, compte tenu des effets indésirables possibles sur le fœtus et le déroulement de la grossesse. Au troisième trimestre, ce traitement est déconseillé, car il contribue à une diminution de la contractilité utérine (travail prolongé) et peut provoquer des saignements importants. Le fœtus peut présenter une hypertension pulmonaire et une insuffisance rénale.
Les effets secondaires du médicament incluent des symptômes gastro-intestinaux (dyspepsie, douleurs épigastriques et abdominales, risque de saignement gastrique avec développement d'une anémie ferriprive). Des saignements de nez, des saignements des gencives et des organes urinaires sont possibles.
Un surdosage peut provoquer des étourdissements, des évanouissements et des bourdonnements d'oreilles. Les réactions allergiques ne sont pas rares, notamment en cas d'hypersensibilité aux salicylates. Cependant, l'anaphylaxie et l'insuffisance respiratoire sont des effets secondaires rares.
Le choix des médicaments utilisés en thérapie complexe et les posologies recommandées doivent être strictement individuels. Une prudence particulière est de mise chez les femmes enceintes, les mères allaitantes, les enfants et les personnes âgées.
Médecine traditionnelle et homéopathie
La fibroélastose cardiaque est une maladie grave et sévère, caractérisée par une évolution progressive et pratiquement sans chance de guérison. Il est évident qu'un traitement efficace par des remèdes populaires est impossible. Les recettes de la médecine traditionnelle, principalement à base de plantes, ne peuvent être utilisées qu'en complément et uniquement avec l'autorisation d'un médecin, afin de ne pas aggraver un pronostic déjà sombre.
Quant aux remèdes homéopathiques, leur utilisation n'est pas interdite et peut s'inscrire dans un traitement global de l'insuffisance cardiaque. Cependant, dans ce cas précis, il ne s'agit pas tant de traitement que de prévention de la progression de l'ICC.
Les médicaments doivent être prescrits par un homéopathe expérimenté, et la question de la possibilité de les inclure dans une thérapie complexe relève de la compétence du médecin traitant.
Quels médicaments homéopathiques aident à retarder la progression de l'insuffisance cardiaque dans la fibroélastose? En cas d'insuffisance cardiaque aiguë, les homéopathes ont recours aux médicaments suivants: Arsenicum album, Antimonium tartaricum, Carbo vegetabilis et Acidum oxalicum. Malgré la similitude des indications, pour choisir un médicament efficace, les médecins se basent sur les manifestations externes de l'ischémie, à savoir la cyanose (son degré et sa prévalence), et sur la nature du syndrome douloureux.
En cas d'ICC, les médicaments suivants peuvent être inclus dans le traitement d'entretien: Lachesis et Nayu, Lycopus (dans les stades initiaux de l'hypertrophie cardiaque), Laurocerasus (pour l'essoufflement au repos), Latrodectus mactans (pour les pathologies valvulaires), préparations d'aubépine (particulièrement utiles pour les lésions endomyocardiques).
En cas de battements cardiaques forts, les médicaments suivants peuvent être prescrits pour le traitement symptomatique: Spigelia, Glonoinum (pour la tachycardie), Aurum metallicum (pour l'hypertension).
Pour réduire l'essoufflement, les plantes suivantes peuvent être utilisées: Grindelia, Spongia et Lahegis. Pour soulager les douleurs cardiaques, on peut prescrire: Cactus, Cereus, Naya, Cuprum, et pour soulager l'anxiété, Aconitum. En cas d'asthme cardiaque, les plantes suivantes sont indiquées: Digitalis, Laurocerasus, Lycopus.
La prévention
La prévention de la fibroélastose acquise du cœur et des poumons consiste à prévenir et à traiter rapidement les maladies infectieuses et inflammatoires, notamment celles qui touchent les organes vitaux. Un traitement efficace de la maladie sous-jacente permet d'éviter des conséquences dangereuses, notamment la fibroélastose. C'est une excellente raison de prendre soin de sa santé et de celle des générations futures, ce qui contribue à un avenir sain et à la longévité.
Prévoir
Les modifications du tissu conjonctif associées à la fibroélastose cardiaque et pulmonaire sont considérées comme irréversibles. Bien que certains médicaments puissent réduire quelque peu l'épaisseur de l'endocarde grâce à un traitement à long terme, ils ne garantissent pas la guérison. Bien que la maladie ne soit pas toujours mortelle, le pronostic reste relativement sombre. Le taux de survie à 4 ans est de 77 %. [ 14 ]
Le pronostic le plus sombre, comme nous l'avons déjà mentionné, concerne la forme congénitale de fibroélastose cardiaque, dont les manifestations d'insuffisance cardiaque sont visibles dès les premières semaines et les premiers mois de vie de l'enfant. Seule une transplantation cardiaque peut sauver le bébé, opération risquée à un stade aussi précoce, et qui doit être réalisée avant l'âge de 2 ans. Ces enfants ne vivent généralement pas plus longtemps.
D'autres opérations permettent seulement d'éviter la mort prématurée de l'enfant (et pas toujours), mais ne peuvent pas le guérir complètement de l'insuffisance cardiaque. La mort survient avec décompensation et développement d'une insuffisance respiratoire.
Le pronostic de la fibroélastose pulmonaire dépend des caractéristiques de la maladie. Si les symptômes apparaissent rapidement, le risque est extrêmement faible. Si la maladie progresse progressivement, l'espérance de vie du patient est d'environ 10 à 20 ans, jusqu'à l'apparition d'une insuffisance respiratoire due à des modifications des alvéoles pulmonaires.
De nombreuses pathologies difficiles à traiter peuvent être évitées grâce à des mesures préventives. Dans le cas de la fibroélastose cardiaque, il s'agit avant tout de prévenir les facteurs susceptibles d'affecter le développement du cœur et du système circulatoire du fœtus (à l'exception des prédispositions héréditaires et des mutations, contre lesquelles les médecins sont impuissants). Si ces facteurs ne peuvent être évités, un diagnostic précoce permet d'identifier la pathologie à un stade où l'interruption de grossesse est possible, ce qui est considéré comme humanitaire dans ce cas.

