Expert médical de l'article
Nouvelles publications
La thérapie par cellules souches est efficace dans le traitement de l'insuffisance cardiaque
Dernière revue: 01.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
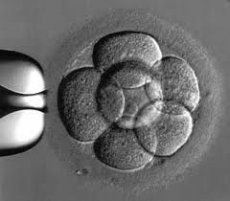
La thérapie par cellules souches dans le traitement des patients atteints d’insuffisance cardiaque de classe III et IV s’est révélée prometteuse dans la prévention des complications graves et du décès.
La société australienne Mesoblast Ltd a déclaré que la thérapie par cellules souches s'était avérée sûre dans le traitement de l'insuffisance cardiaque et était capable de réduire le risque de complications graves telles que la crise cardiaque et la mort cardiaque subite de 78 % sur un an par rapport aux patients ayant reçu un traitement standard.
Les résultats de l’étude, qui a porté sur 60 patients, ont été présentés lors de la conférence de l’American Heart Association à Orlando.
« Il est extrêmement surprenant et vraiment incroyable que cette thérapie ait pu réduire le risque de décès et de complications graves de l'insuffisance cardiaque sur une période de suivi de trois ans », a déclaré le Dr Emerson Perin, auteur de l'étude et membre du Texas A&M Institute à Houston.
« Si les résultats démontrent l’efficacité du traitement dans une étude plus vaste, nous pensons que nous avons toutes les chances d’obtenir l’approbation de la thérapie par cellules souches au niveau législatif », a déclaré Perin.
Mesoblast et son partenaire Teva Pharmaceutical Industries prévoient de commencer à recruter des patients dans un essai clinique de phase III au cours du premier semestre de l'année prochaine.
La sécurité est l'objectif principal de cette étude. Aucun effet secondaire lié au traitement par cellules souches n'a été signalé pendant toute la durée de l'étude, selon les responsables de Mesoblast.
Comment s'est déroulé le traitement par cellules souches?
Les chercheurs étudient les cellules souches provenant de nombreuses sources depuis plus d’une décennie dans l’espoir que leur capacité à se transformer en une grande variété d’autres types de cellules pourrait aider à traiter de nombreux types de maladies, des lésions de la moelle épinière aux maladies cardiaques.
Le mésoblaste utilise des cellules souches dérivées de la moelle osseuse, appelées cellules progénitrices mésenchymateuses. Ces cellules sont acheminées directement vers le cœur par un cathéter, où elles stimulent la croissance des vaisseaux sanguins.
Étant donné que les cellules sont extraites d’un donneur non apparenté, les patients doivent être examinés pour s’assurer qu’ils ne produisent pas d’anticorps contre les greffes.
Aucun des patients souffrant d’insuffisance cardiaque ayant reçu les cellules n’a développé d’hypersensibilité ou de niveaux significatifs d’anticorps contre les cellules, de sorte qu’aucune réponse immunitaire significative n’a été observée.
Les patients de l'étude souffraient d'insuffisance cardiaque modérée à sévère, caractérisée par une capacité réduite du muscle cardiaque à pomper le sang. La fraction d'éjection était inférieure à 40 %, alors que chez une personne en bonne santé, elle devrait être supérieure à 55 %.
Le traitement par cellules souches n’a pas entraîné d’amélioration significative de la fraction d’éjection, mais une tendance à l’amélioration a été observée lors du test de marche de six minutes, signe que les patients se sentaient mieux.
Les scientifiques ont testé trois doses, ou concentrations, de cellules – 25 millions de cellules, 75 millions de cellules et 150 millions de cellules – chez 15 patients de chaque groupe. L'étude incluait également 15 patients supplémentaires recevant des traitements standard contre l'insuffisance cardiaque. Au vu des résultats de l'étude de phase II, les entreprises ont annoncé leur intention d'étendre l'essai à la dose de 150 millions de cellules.


 [
[