Nouvelles publications
Clarification des mécanismes cellulaires de la parodontite grâce à un modèle animal amélioré
Dernière revue: 02.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
Des chercheurs de l'Université médicale et dentaire de Tokyo (TMDU) ont développé une technique qui permet une analyse détaillée du développement de la parodontite au fil du temps.
La maladie parodontale, appelée parodontite, est la principale cause de perte de dents et touche près d'un adulte sur cinq dans le monde. Dans la plupart des cas, cette affection résulte d'une réaction inflammatoire à une infection bactérienne des tissus entourant les dents.
À mesure que la maladie s'aggrave, les gencives commencent à se rétracter, exposant les racines des dents et l'os. L'incidence de la parodontite augmente avec l'âge et, compte tenu de l'allongement de la durée de vie mondiale, il est important de bien comprendre ses causes sous-jacentes et son évolution.
Dans une étude publiée dans la revue Nature Communications, des chercheurs du TMDU ont trouvé un moyen d’atteindre cet objectif en améliorant un modèle animal largement utilisé pour étudier la parodontite.
Il est difficile d'étudier directement la parodontite chez l'homme. Par conséquent, les scientifiques ont souvent recours à des modèles animaux pour les études précliniques. Par exemple, le « modèle murin de parodontite induite par ligature » a permis aux chercheurs d'étudier les mécanismes cellulaires sous-jacents à cette maladie depuis son introduction en 2012.
En termes simples, ce modèle induit artificiellement une maladie parodontale en plaçant des fils de soie sur les molaires de souris, provoquant ainsi l'accumulation de plaque. Bien que cette méthode soit pratique et efficace, elle ne permet pas de saisir l'intégralité de la parodontite.
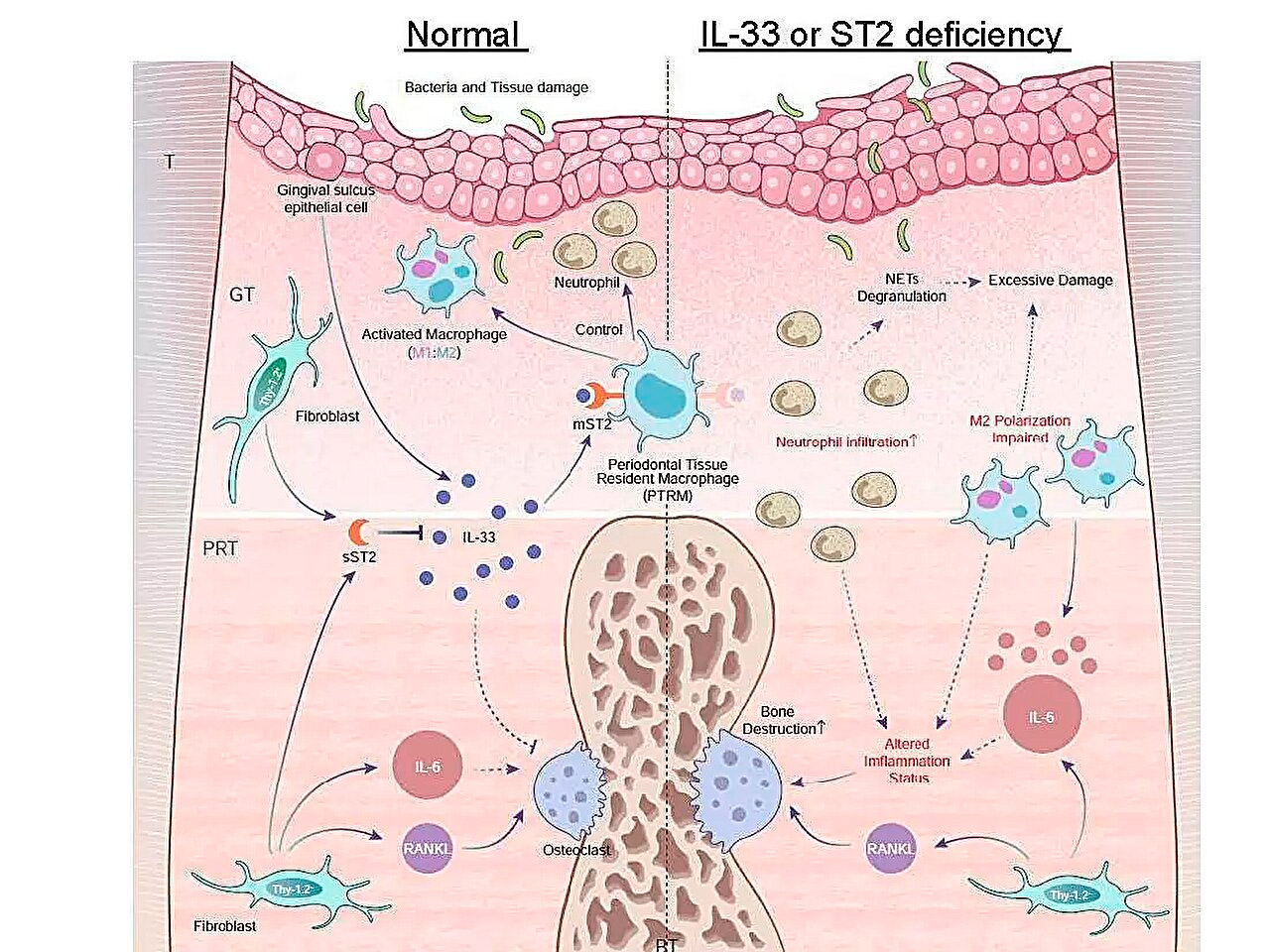
Illustration schématique des profils d'expression des gènes inflammatoires au cours de la parodontite et du rôle de l'axe IL-33/ST2 dans la lutte contre l'inflammation aiguë. Source: Université médicale et dentaire de Tokyo.
« Bien que le tissu parodontal soit composé de gencive, de ligament parodontal, d'os alvéolaire et de cément, l'analyse est généralement réalisée uniquement sur des échantillons de gencive en raison de limitations techniques et quantitatives », note Anhao Liu, auteur principal de l'étude. « Cette stratégie d'échantillonnage limite les conclusions que l'on peut tirer de ces études; il est donc nécessaire de recourir à des méthodes permettant l'analyse simultanée de tous les composants tissulaires. »
Pour pallier cette limitation, l'équipe de recherche a développé un modèle modifié de parodontite induite par ligature. Au lieu de la ligature simple classique, ils ont utilisé une triple ligature sur la molaire supérieure gauche de souris mâles. Cette stratégie a permis d'élargir la zone de perte osseuse sans détruire significativement l'os autour de la deuxième molaire, augmentant ainsi le nombre de types de tissus parodontaux différents.
« Nous avons isolé trois principaux types de tissus et évalué le rendement en ARN entre les deux modèles. Les résultats ont montré que le modèle à triple ligature augmentait efficacement le rendement, atteignant quatre fois la quantité de tissu périradiculaire normal et permettant une analyse haute résolution de différents types de tissus », explique le Dr Mikihito Hayashi, auteur principal.
Après avoir confirmé l’efficacité de leur modèle modifié, les chercheurs ont entrepris d’étudier les effets de la parodontite sur l’expression des gènes dans différents types de tissus au fil du temps, en se concentrant sur les gènes associés à l’inflammation et à la différenciation des ostéoclastes.
L'une de leurs principales découvertes a été que l'expression du gène Il1rl1 était significativement plus élevée dans le tissu périradiculaire cinq jours après la ligature. Ce gène code la protéine ST2 dans les isoformes récepteur et leurre, qui se lie à une cytokine appelée IL-33, impliquée dans les processus inflammatoires et immunorégulateurs.
Afin de mieux comprendre le rôle de ce gène, l'équipe a induit une parodontite chez des souris génétiquement modifiées dépourvues des gènes Il1rl1 ou Il33. Ces souris ont présenté une destruction osseuse inflammatoire accélérée, soulignant le rôle protecteur de la voie IL-33/ST2. Une analyse plus approfondie des cellules contenant la protéine ST2 sous sa forme réceptrice, mST2, a révélé que la plupart d'entre elles provenaient de macrophages.
« Les macrophages sont généralement classés en deux types principaux, pro-inflammatoires et anti-inflammatoires, selon leur activation. Nous avons découvert que les cellules exprimant mST2 étaient uniques en ce sens qu'elles exprimaient simultanément certains marqueurs des deux types de macrophages », a commenté le Dr Takanori Iwata, auteur principal. « Ces cellules étaient présentes dans le tissu périradiculaire avant le début de l'inflammation, c'est pourquoi nous les avons appelées “macrophages résidents du tissu parodontal”. »
Ensemble, les résultats de cette étude démontrent la puissance d’un modèle animal modifié pour étudier la parodontite à une échelle plus détaillée, jusqu’au niveau biomoléculaire.
« Nous suggérons l'existence d'une nouvelle voie moléculaire IL-33/ST2 régulant l'inflammation et la destruction osseuse dans les maladies parodontales, ainsi que de macrophages spécifiques du tissu périradiculaire, fortement impliqués dans les maladies parodontales. Nous espérons que cela conduira au développement de nouvelles stratégies de traitement et de nouvelles méthodes de prévention », conclut le Dr Tomoki Nakashima, auteur principal.
