Nouvelles publications
Une nouvelle étude révèle le rôle clé des protéines mitochondriales dans la régénération du cœur
Dernière revue: 02.07.2025

Tout le contenu iLive fait l'objet d'un examen médical ou d'une vérification des faits pour assurer autant que possible l'exactitude factuelle.
Nous appliquons des directives strictes en matière d’approvisionnement et ne proposons que des liens vers des sites de médias réputés, des instituts de recherche universitaires et, dans la mesure du possible, des études évaluées par des pairs sur le plan médical. Notez que les nombres entre parenthèses ([1], [2], etc.) sont des liens cliquables vers ces études.
Si vous estimez qu'un contenu quelconque de notre contenu est inexact, obsolète ou discutable, veuillez le sélectionner et appuyer sur Ctrl + Entrée.
Les mitochondries jouent un rôle essentiel dans la fourniture de l'énergie nécessaire au bon fonctionnement cellulaire. Dans les mitochondries, l'énergie est produite par la chaîne respiratoire, composée de cinq complexes, appelés CI-CV. Ces complexes peuvent s'assembler en supercomplexes, mais le rôle de ce processus et son contrôle sont mal connus.
Cette nouvelle étude examine les mécanismes d'assemblage des supercomplexes et révèle un impact significatif des facteurs d'assemblage mitochondrial sur la régénération du tissu cardiaque. Elle a été codirigée par le Dr José Antonio Enríquez du Centre national de recherche cardiovasculaire (CNIC) et le Dr Nadia Mercader de l'Université de Berne (Suisse), chercheuse invitée au CNIC.
Une étude publiée dans la revue Developmental Cell montre que le membre de la famille de protéines Cox7a joue un rôle fondamental dans l'assemblage des dimères CIV et que cet assemblage est essentiel au bon fonctionnement des mitochondries et donc à la production d'énergie cellulaire.
La famille des protéines Cox7a comprend trois membres: Cox7a1, Cox7a2 et Cox7a2l (également appelée SCAF1). Des études antérieures menées par les deux groupes ont montré que lorsque le CIV contient SCAF1, il s'associe fortement au CIII, formant un supercomplexe respiratoire appelé respirasome. Dans ces études, les auteurs ont émis l'hypothèse que l'inclusion de Cox7a2 entraînerait une CIV incapable de s'associer, tandis que les molécules CIV contenant Cox7a1 s'associeraient pour former des homodimères CIV. Cette nouvelle étude démontre expérimentalement le rôle de Cox7a1 dans la formation de ces homodimères CIV.
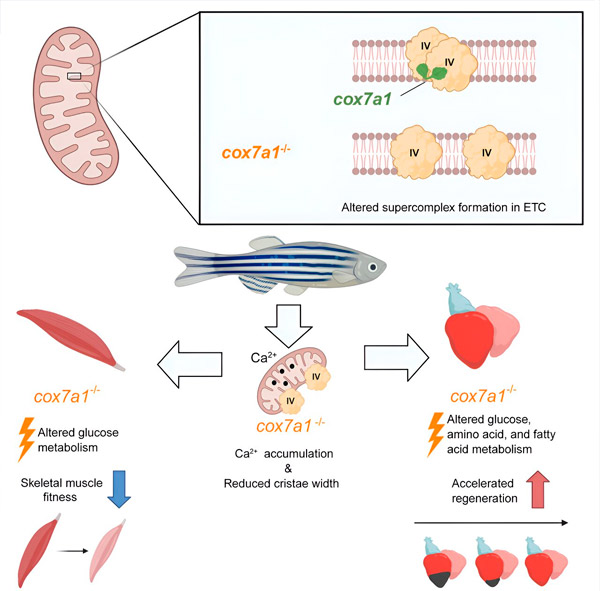
Cellule de développement (2024). DOI: 10.1016/j.devcel.2024.04.012
En travaillant sur un modèle de poisson zèbre, les chercheurs ont découvert que l’absence de Cox7a1 empêchait la formation de dimères CIV, et que la perte de ces dimères affectait le poids et la capacité de nage des poissons affectés.
« La Cox7a1 est principalement exprimée dans les cellules musculaires striées, et c'est le tissu musculaire squelettique qui a le plus souffert de l'absence de fonction de la Cox7a1. L'autre type majeur de muscle strié est le muscle cardiaque, ou myocarde », a expliqué le Dr Enriquez.
Cependant, alors que la perte de Cox7a1 dans le muscle squelettique était préjudiciable, son absence dans le muscle cardiaque améliorait la réponse régénératrice cardiaque aux blessures.
« Ce résultat montre que ces protéines jouent un rôle clé dans l'activation de la capacité du cœur à se réparer après une blessure », a expliqué la première auteure de l'étude, Carolina Garcia-Pojatos.
Afin d'explorer plus en détail la fonction de Cox7a1, les chercheurs du CNIC Enrique Calvo et Jesús Vásquez ont mené une étude protéomique du muscle squelettique et du myocarde chez des poissons zèbres dépourvus de Cox7a1. Cette analyse a été complétée par une étude métabolomique menée par des collègues de l'Université de Berne. Cette analyse combinée a révélé des différences significatives par rapport aux poissons non modifiés présentant une expression intacte de Cox7a1.
« Ces résultats suggèrent que les molécules impliquées dans l'assemblage des supercomplexes mitochondriaux peuvent avoir des effets significatifs sur le contrôle métabolique, ouvrant peut-être la voie à de nouveaux traitements pour les maladies cardiaques et d'autres affections métaboliques », a déclaré le Dr Mercader.
Selon l'équipe de recherche, cette découverte représente « une avancée significative dans la compréhension des mécanismes cellulaires impliqués dans la régénération cardiaque et pourrait ouvrir la voie au développement de thérapies visant à stimuler la régénération cardiaque ».
Les auteurs concluent que les facteurs d’assemblage mitochondrial peuvent influencer de manière significative le contrôle métabolique.
